研究背景
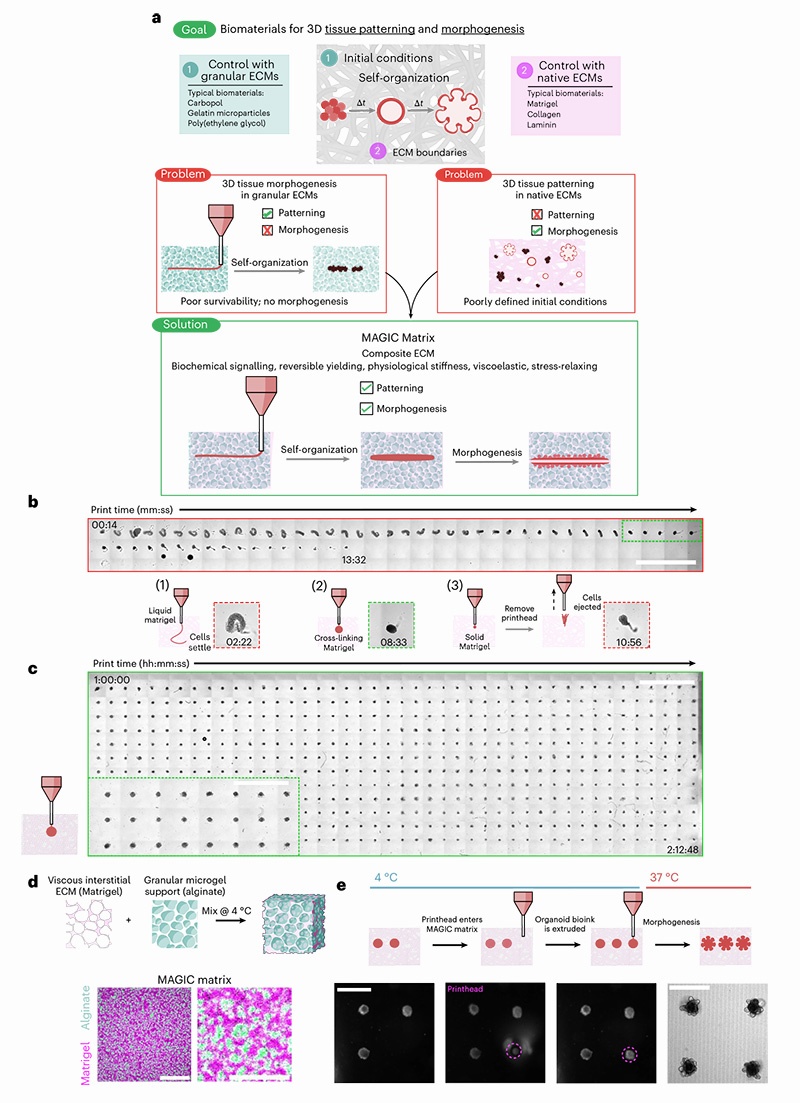
体外培养组织的均一性和复杂性控制一直是组织工程领域的核心挑战。体内组织的自组织依赖于动态变化的相邻组织和细胞外基质(ECM)边界,而现有生物材料难以同时满足精确控制初始培养条件和模拟动态组织边界这两个关键需求。
1. 经典金标准材料的局限性
Matrigel等重组基底膜基质(rBMs)虽能支持类器官自组织,但存在致命缺陷:
-
打印窗口极窄(仅约2分钟),无法支持长时间高精度打印
-
凝胶化后弹性过高,细胞难以挤出或被挤出打印平面
-
初始条件难以控制,导致类器官异质性极高
2. 现有打印材料的不足
-
传统颗粒微凝胶虽具有可逆屈服应力特性,适合嵌入式3D打印,但长期细胞存活率低,无法支持复杂组织形态发生
-
添加胶原等间质基质虽能改善细胞存活,但会改变材料流变学性质,抑制上皮组织生长和形态发生
3. 关键科学问题
生物材料的生物力学性质与组织形态发生结果之间的定量关系尚不明确,特别是长时程、大应变下的力学行为对类器官发育的影响从未被系统研究。
研究内容
1. MAGIC基质的设计与制备
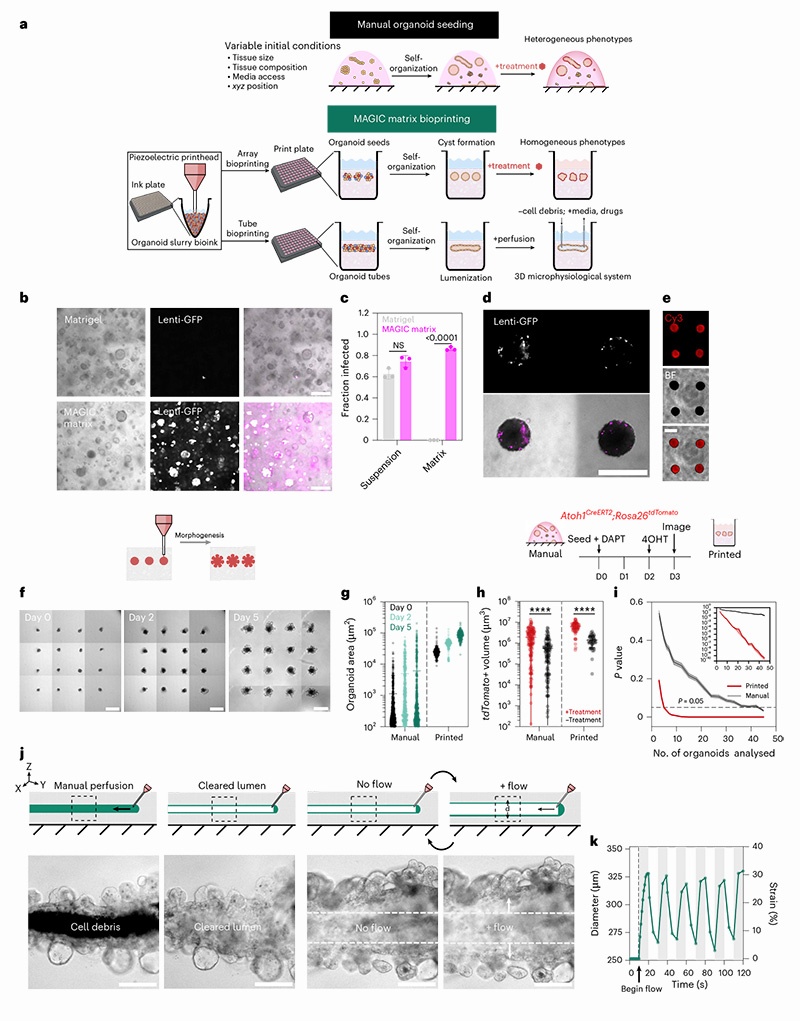
研究人员开发了一种名为Matrigel-海藻酸钠颗粒-间质复合物(MAGIC)基质的新型颗粒生物材料,完美解决了打印性能与生物功能之间的矛盾。
1.1 实验配方
|
组分
|
浓度/比例
|
作用
|
|
海藻酸钠(Sigma 9005-38-3)
|
0.5 wt%(最优)/1 wt%
|
提供颗粒支撑相,光学透明,生物惰性
|
|
碳酸钙
|
0.1 wt%
|
钙离子源,用于海藻酸钠交联
|
|
冰醋酸
|
1:500(体积比)
|
缓慢释放钙离子,触发微凝胶形成
|
|
生长因子减少型Matrigel(Corning 354230)
|
与AMG浆液1:1(体积比,最优)
|
提供生物化学信号,支持类器官形态发生
|
|
DMEM:F12培养基
|
用于微凝胶洗涤和重悬
|
维持渗透压和pH
|
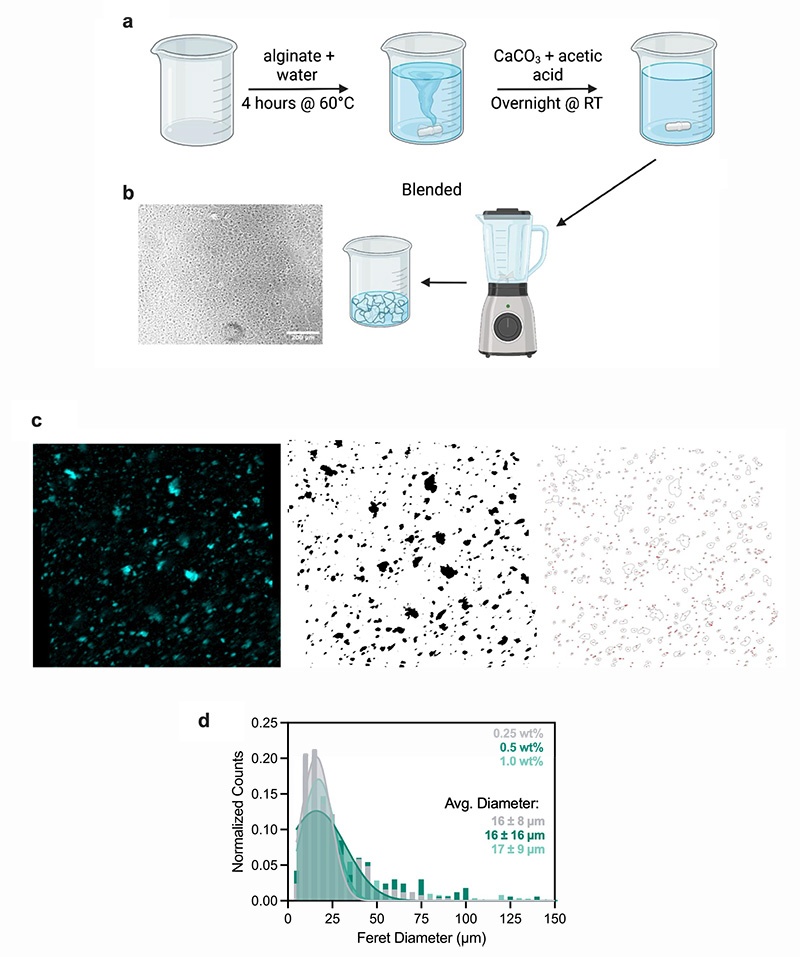
1.2 详细制备步骤
海藻酸钠微凝胶(AMG)制备
-
将1g海藻酸钠溶解于100ml 60℃无菌双蒸水中,搅拌2-4小时至完全均匀
-
加入200mg碳酸钙,冷却至室温后继续搅拌1小时
-
缓慢滴加400μl冰醋酸(1:500比例),1000rpm搅拌过夜,形成微凝胶
-
次日用商用搅拌机高速搅拌60秒,通过100μm滤网去除大颗粒
-
20000g、4℃离心20分钟,弃上清,用含抗生素的DMEM:F12重悬,4℃过夜
-
使用前再次离心,弃上清,得到浓缩的微凝胶浆液
MAGIC基质制备
-
使用前将浓缩AMG浆液与液态Matrigel在4℃下按1:1体积比充分混合
-
保持4℃低温直至打印或接种完成
-
接种/打印后转移至37℃ CO₂培养箱孵育5-10分钟,使Matrigel交联固化
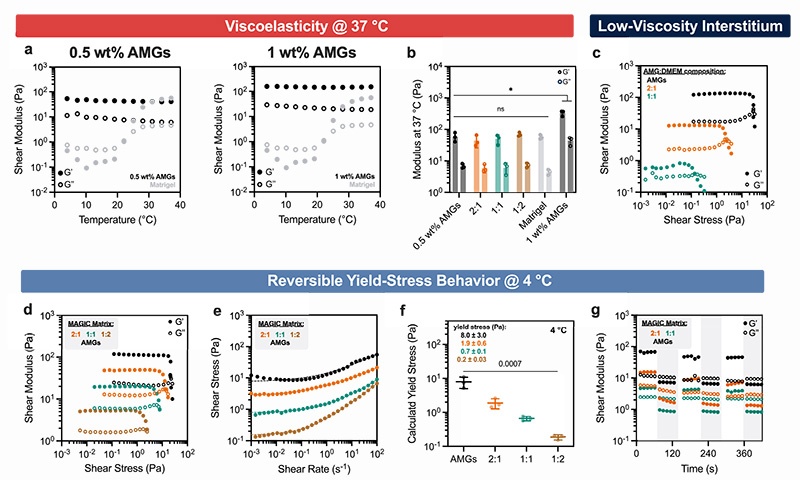
2. MAGIC基质的流变学特性与形态发生关系
研究人员系统表征了不同组成MAGIC基质的流变学性质,并建立了其与肠道类器官形态发生的定量关系。
关键发现
-
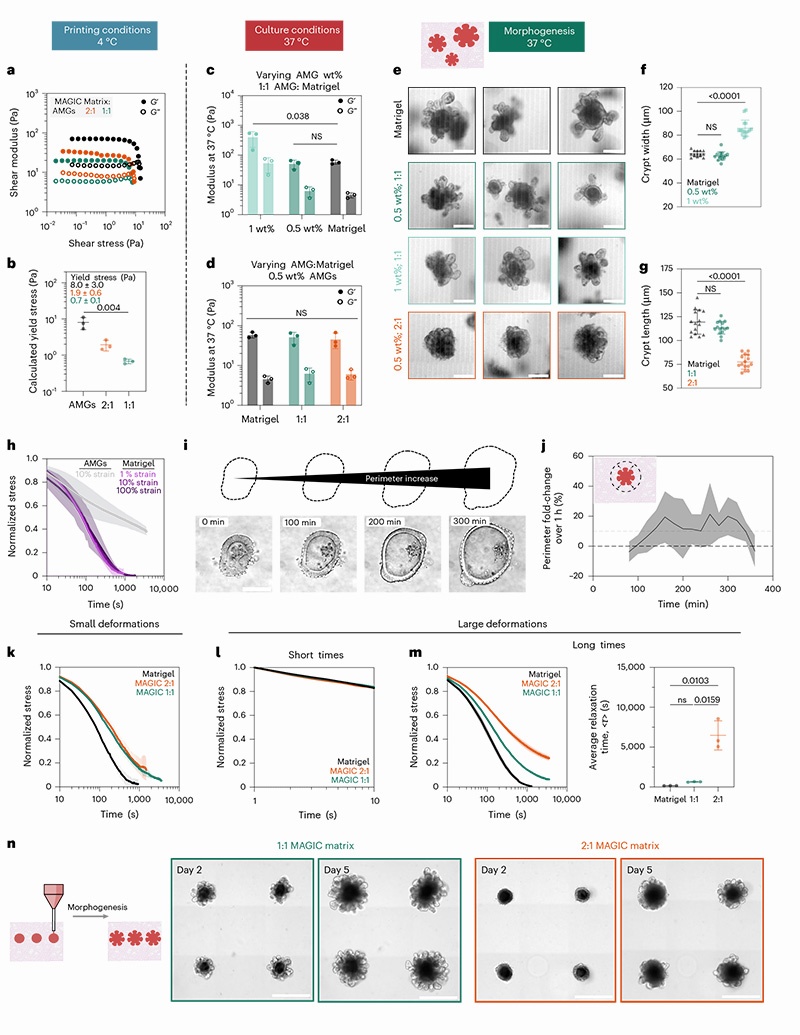
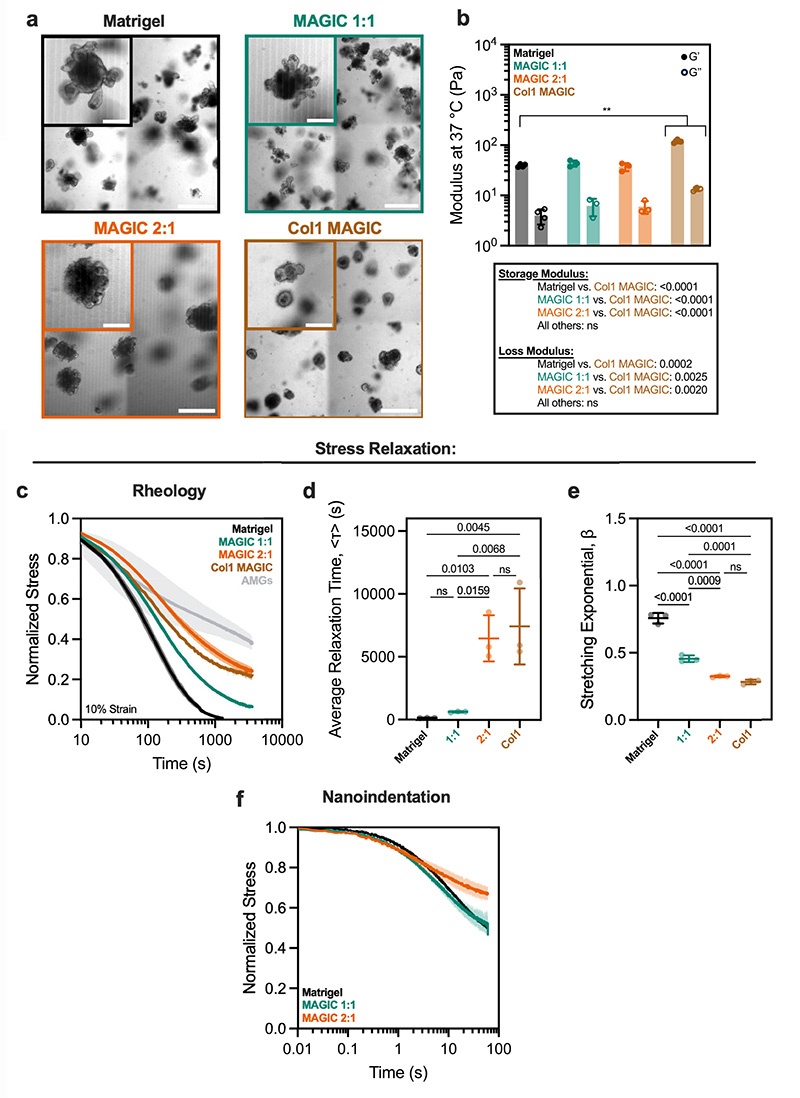
4℃打印特性:所有MAGIC基质组成均表现出可逆屈服应力行为,符合Herschel-Bulkley模型,屈服应力可通过改变AMG与Matrigel比例在一个数量级范围内调节
-
37℃培养特性:0.5 wt% AMG与Matrigel 1:1混合的MAGIC基质,其储能模量(G')和损耗模量(G'')与纯Matrigel几乎完全一致
-
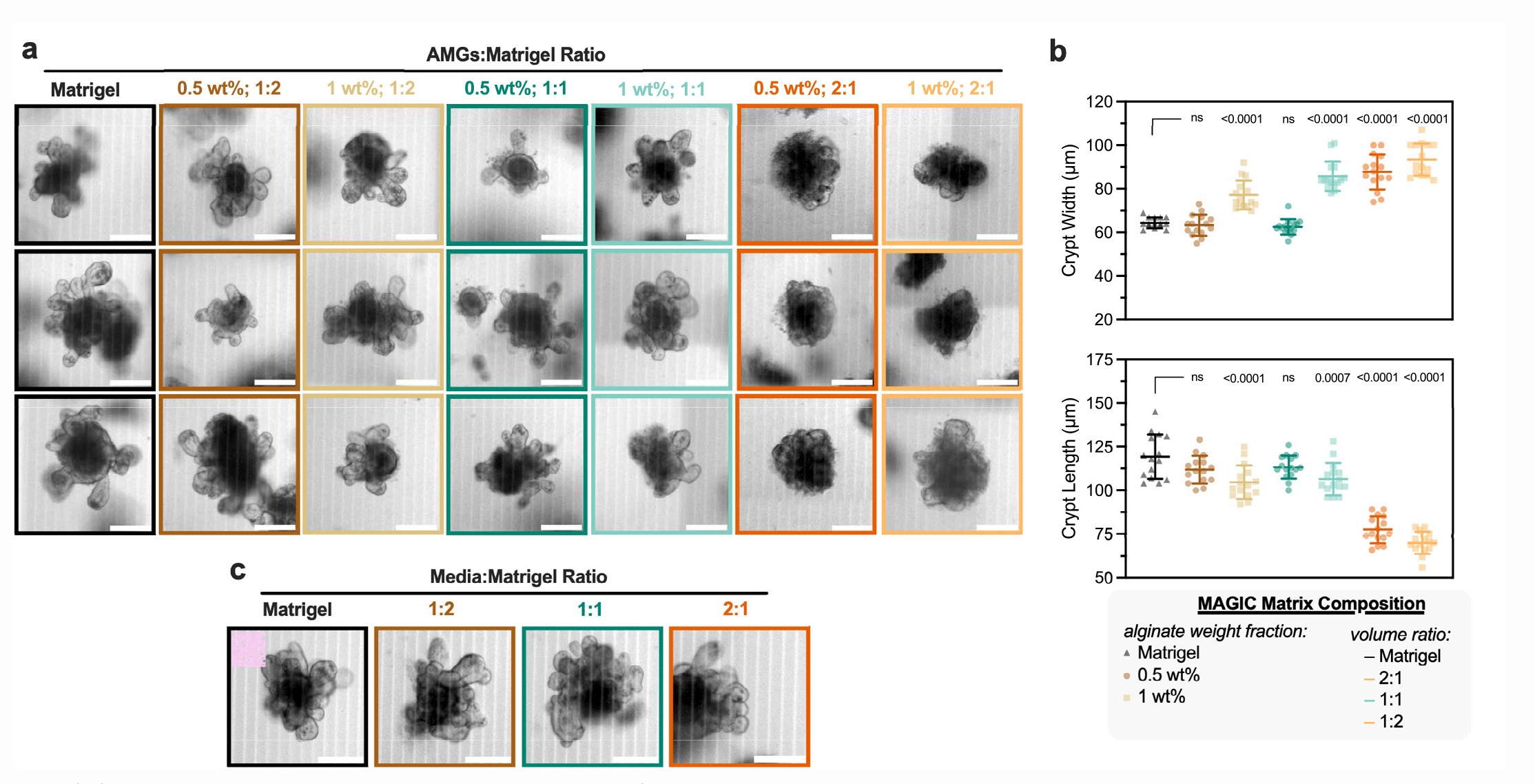
应力松弛的决定性作用:当短时间尺度、小应变下的模量相同时,长时间尺度(小时级)、大应变(10%)下的应力松弛速率和程度是决定类器官形态发生的关键参数
-
1:1 MAGIC基质在10%应变下1小时内可松弛95%的内部应力,残留应力仅约0.2 Pa
-
2:1 MAGIC基质应力松弛显著减慢,导致肠道类器官隐芽变短变宽,形态发生异常
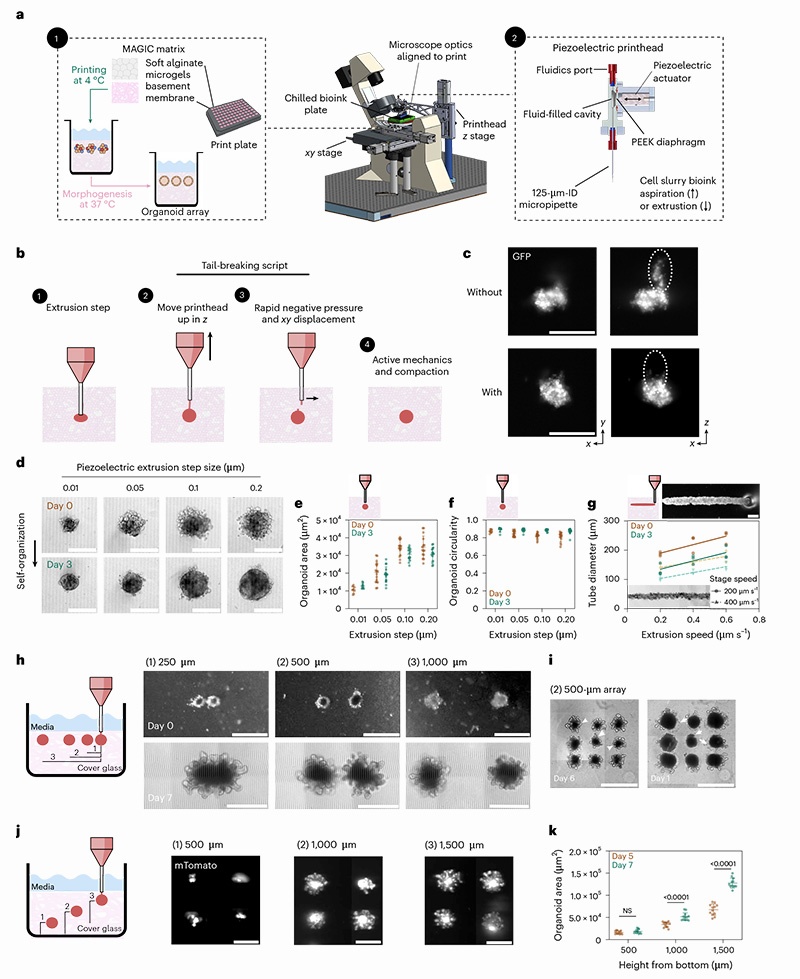
为充分发挥MAGIC基质的优势,研究人员设计了一款专用直写式(DIW)3D打印压电打印头,实现了高密度细胞悬液(≥10⁸ cells/ml)的精准、自动化打印。
打印平台核心参数
-
体积分辨率:~10 pl
-
最大抽吸/挤出体积:~660 nl
-
最大理论速率:~300 μs⁻¹
-
喷嘴规格:125 μm内径塑料微管(可选75 μm或200 μm)
-
温度控制:打印床保持4-8℃,生物墨水池保持5℃
-
特色功能:实时成像监控、"断尾"脚本(通过快速负压和位移提高打印保真度)
打印流程
-
将解离的类器官细胞制备成高密度细胞悬液(≥10⁸ cells/ml)
-
4℃下将MAGIC基质加入96孔板或腔室载玻片
-
打印头直接从384孔板中抽吸细胞悬液(无死体积)
-
按照预设程序打印类器官阵列或管状结构
-
37℃孵育5-10分钟使基质交联
-
加入预热的组织特异性培养基进行培养
4. 多谱系类器官自组织验证
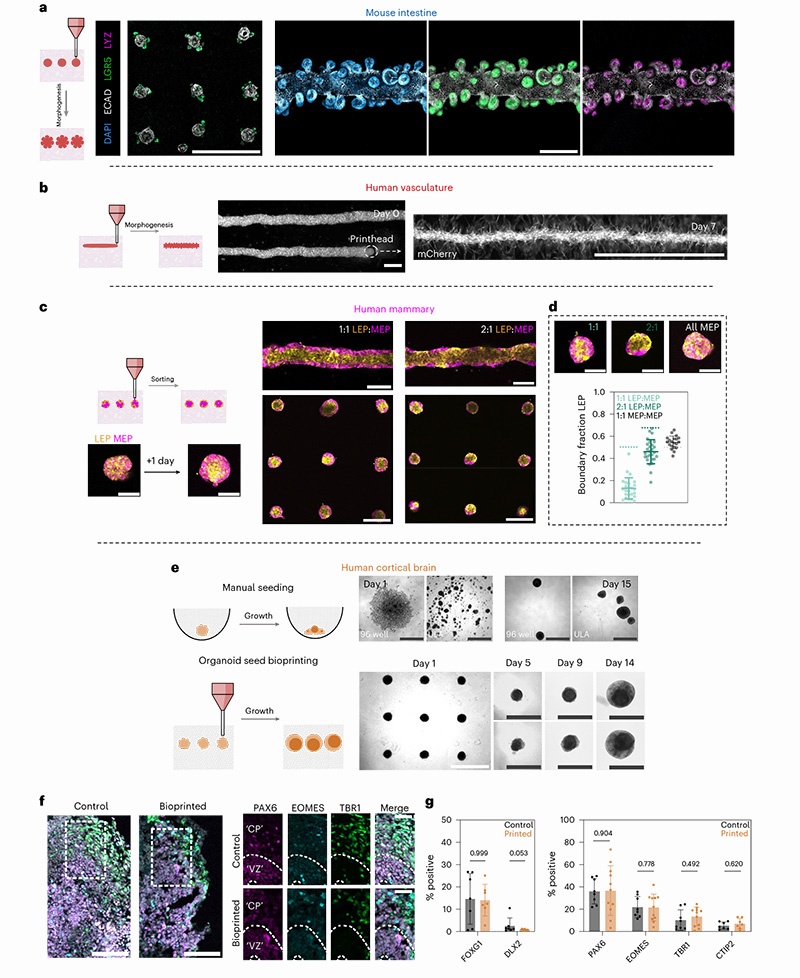
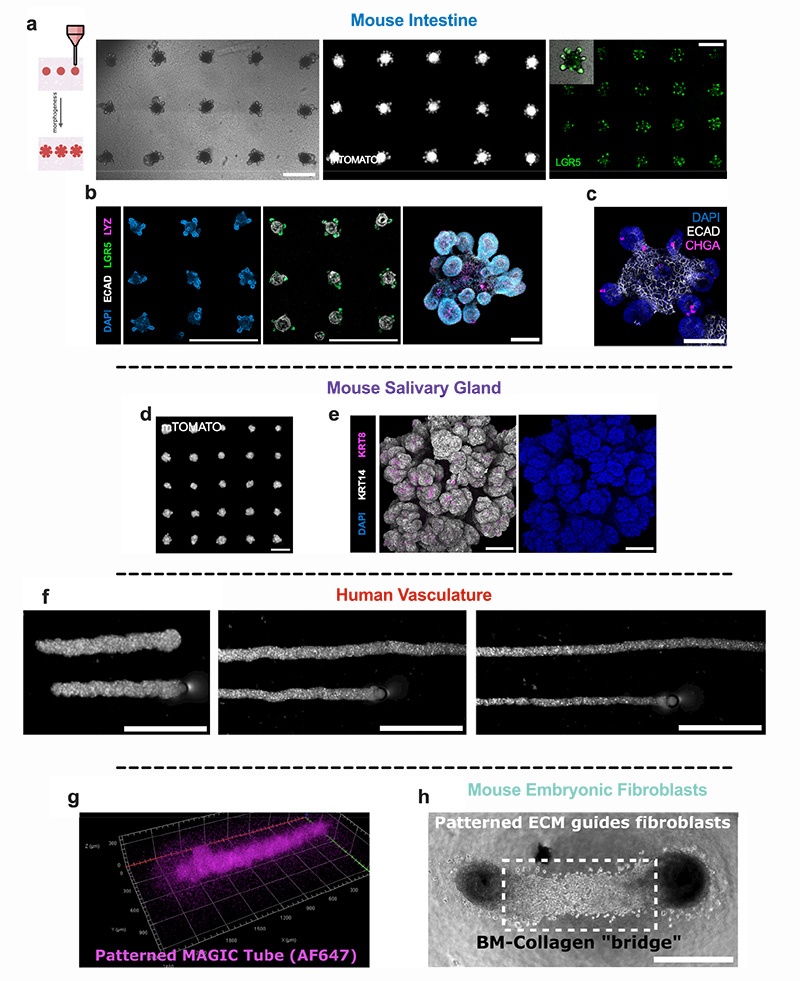
MAGIC基质成功支持了来自三个胚层的多种组织类型的自组织,且表现与纯Matrigel培养无显著差异:
-
内胚层:小鼠肠道类器官(形成典型隐芽-绒毛结构,Lgr5+干细胞定位于隐芽基部)、唾液腺类器官(形成多叶状结构)
-
中胚层:人脐静脉内皮细胞(HUVEC)形成超过2mm长的血管网络并发生出芽
-
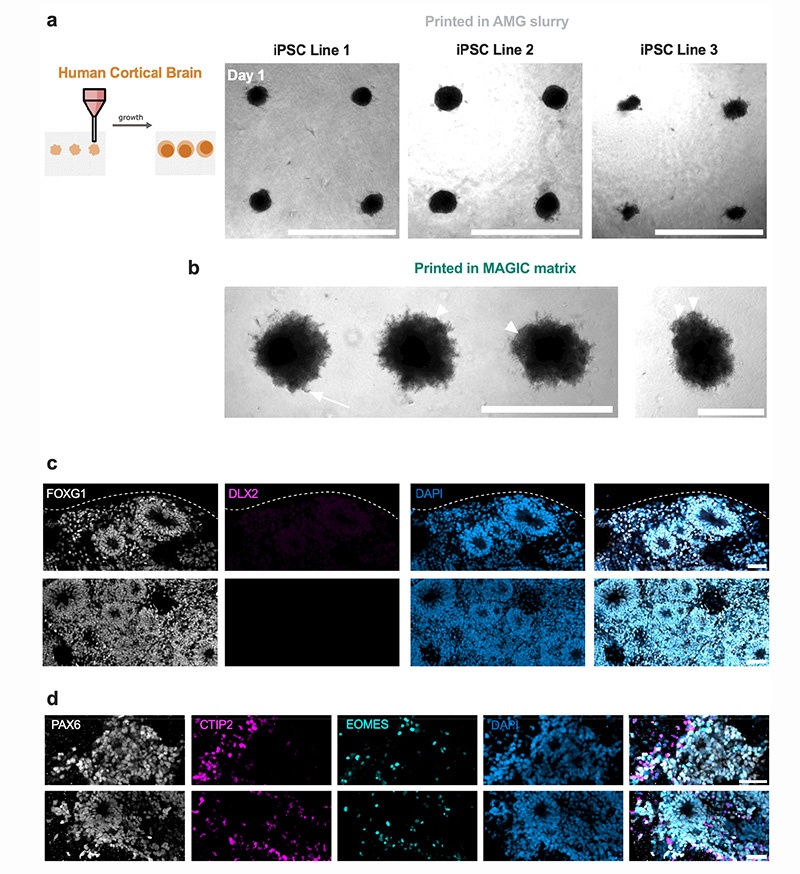
外胚层:人乳腺上皮细胞(HMEC)在1天内完成细胞分选形成双层结构、人诱导多能干细胞(iPSC)来源的皮质脑类器官(形成典型的神经玫瑰花结结构)
5. 高通量类器官阵列与统计效力提升
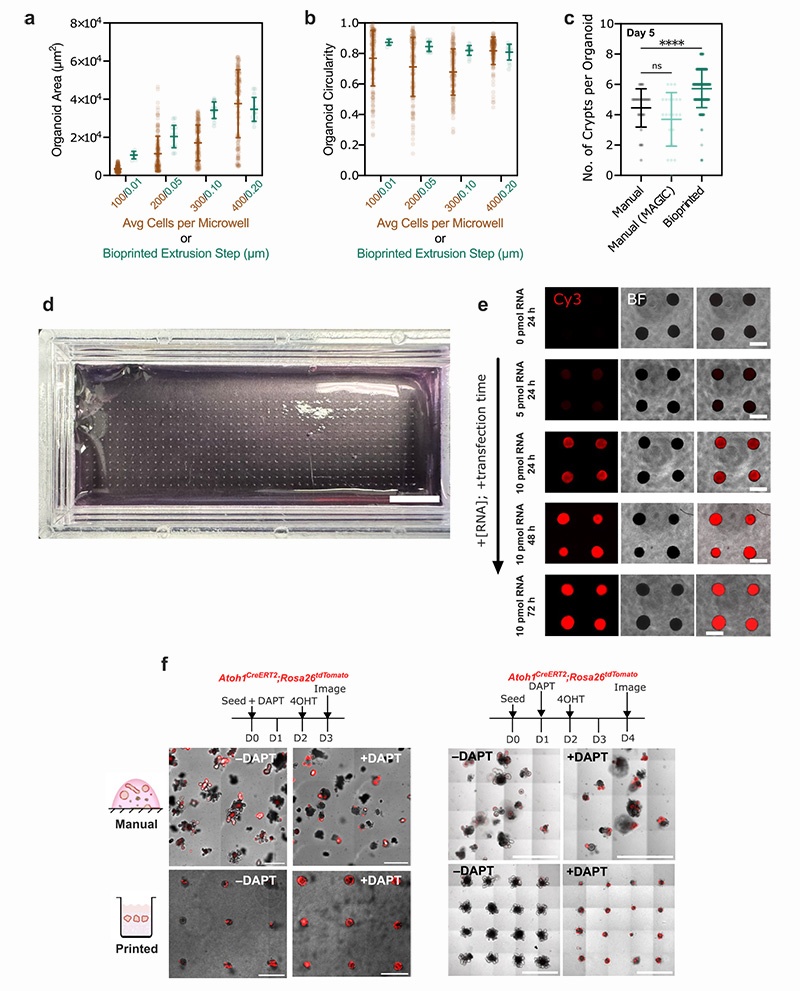
通过精确控制初始条件,MAGIC基质生物打印显著提高了类器官的均一性,大幅提升了表型分析的统计效力:
-
均一性提升:生物打印类器官的初始大小和圆形度变异显著低于微孔板聚集法
-
感染效率提升:通过培养基添加慢病毒进行转导时,MAGIC基质中感染效率接近90%,而Matrigel中几乎无感染
-
统计效力提升:
-
生物打印类器官的变异系数仅为48-58%,而手动接种类器官高达127-174%
-
检测相同表型仅需12个生物打印样本,而手动接种需要100个样本
-
45个生物打印样本即可达到p≈10⁻¹⁰的统计显著性,而手动接种45个样本仅能达到p=0.05
6. 可灌注3D微生理系统构建
MAGIC基质的高变形性支持生物打印的肠道类器官管进行灌注培养:
-
打印的肠道管在3-7天内完成管腔化和隐芽形成
-
使用玻璃毛细管可穿刺管腔并进行流体灌注,清除内部细胞碎片
-
施加振荡流体流可模拟肠道蠕动的周期性扩张和收缩,管腔径向扩张可达30%
-
该系统为研究流体剪切力、机械拉伸等生物物理因素对肠道功能的影响提供了理想平台
研究结论
-
核心科学发现:长时程(小时级)、大应变(10%)下的应力松弛是类器官最佳形态发生的独立关键参数,这一发现填补了生物材料力学与组织发育之间定量关系的空白。
-
技术突破:开发了MAGIC基质,首次实现了同时支持高精度嵌入式3D打印和金标准类器官自组织的生物材料,解决了组织工程领域长期存在的"打印性能与生物功能不可兼得"的难题。
-
平台创新:配套开发的压电生物打印平台实现了高密度细胞悬液的无死体积、高精度打印,可精确控制类器官的初始大小、形状、位置和细胞组成。
-
应用价值:
-
显著提高了类器官的均一性和成熟度,将表型分析所需样本量减少了近一个数量级,特别适合珍贵的患者来源样本
-
实现了可灌注3D微生理系统的构建,为药物筛选、疾病建模和再生医学研究提供了强大工具
-
该平台具有高度通用性,可支持来自三个胚层的多种组织类型的生物打印和自组织
-
未来展望:MAGIC基质和压电生物打印技术的结合,为构建更复杂、更接近体内真实结构的自组织组织和器官奠定了基础,有望推动再生医学和精准医学的发展。
补充数据图
论文信息
-
标题
-
Stress-relaxing granular bioprinting materials enable complex and uniform organoid self-organization
-
期刊
-
Nature Materials
-
DOI
-
https://doi.org/10.1038/s41563-026-02519-4
-
通讯作者
-
Rafael Gómez-Sjöberg(陈·扎克伯格生物中心)、Zev J. Gartner(加州大学旧金山分校)
-