研究内容与实验方法
一、核心材料的合成与制备(含实验配方与步骤)
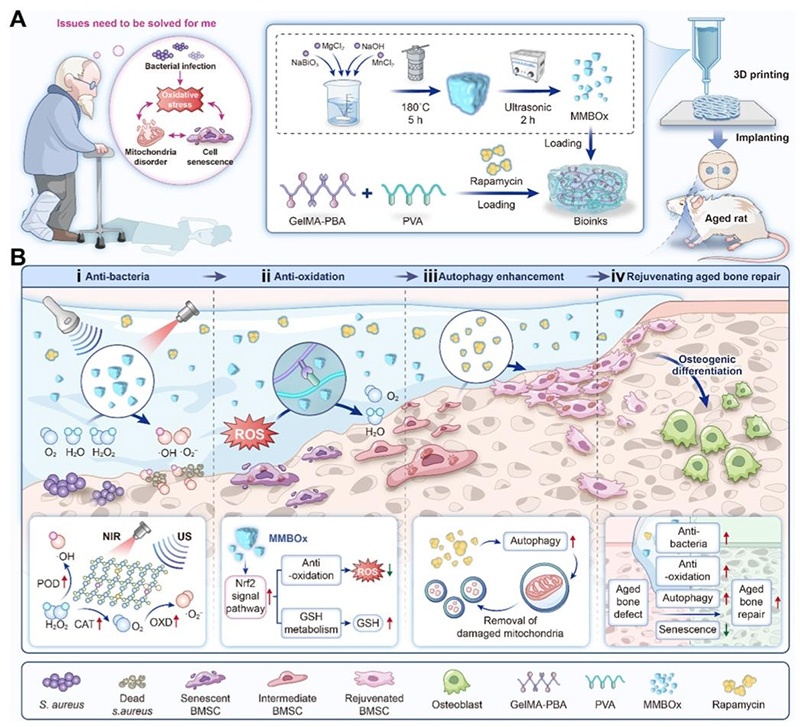
1. MMBOx与BOx纳米颗粒的合成
合成方法:一步水热法
实验配方:
- MMBOx实验组:1.40 g 铋酸钠(NaBiO₃)、1.12 g 氢氧化钠(NaOH)、0.02 g 氯化镁(MgCl₂)、0.04 g 一水合氯化锰(MnCl₂·H₂O),分散于30 mL去离子水中
- BOx对照组:同上配方,不添加MgCl₂与MnCl₂·H₂O
实验步骤:
- 将上述悬浮液室温搅拌2 h,随后转移至聚四氟乙烯内衬的高压反应釜中,180℃水热反应5 h;
- 反应结束自然冷却后,产物经去离子水与无水乙醇交替离心洗涤3次,随后真空干燥12 h;
- 干燥后的产物重新分散于去离子水-乙醇混合液中,冰水浴超声处理4 h;
- 悬浮液先以3000 rpm离心去除大颗粒团聚体,上清液再以8000 rpm离心收集沉淀,真空干燥后得到最终MMBOx/BOx纳米颗粒。
2. ROS响应型3D打印水凝胶支架的制备
步骤1:苯硼酸修饰明胶(GelMA-PBA,GP)的合成
- 将2 mmol DMTMM与2 mmol 4-羧基苯硼酸(4-CPBA)分别溶解于6 mL去离子水与9 mL DMF中;
- 将DMTMM溶液缓慢滴加至4-CPBA溶液中,室温活化30 min;
- 将活化后的4-CPBA溶液逐滴加入2% (w/v) GelMA溶液中,用稀盐酸调节pH至4.5;
- 25℃恒温反应24 h,反应结束后去离子水透析3天,冻干后得到GelMA-PBA产物。
步骤2:生物墨水配方(PBS溶剂体系)
| 组分 | 浓度/含量 | 作用 |
|---|---|---|
| LAP(光引发剂) | 0.25% (w/v) | 蓝光光交联引发剂 |
| GelMA-PBA | 7.5% (w/v) | ROS响应型基质、光交联骨架 |
| PVA | 2.5% (w/v) | 预交联网络、提升打印性能 |
| BOx/MMBOx纳米颗粒 | 5 mg/mL | ROS双向调控、抗菌、声动力/光热功能 |
| 雷帕霉素(Rapa) | 20 μM | 自噬激活、细胞抗衰 |
步骤3:3D打印与支架制备
- 将配制好的生物墨水装入无菌直写式(DIW)生物3D打印机墨盒,通过300 μm喷嘴进行打印,打印环境温度15-20℃,挤出压力0.05-0.15 MPa,接收平台温度控制在8-12℃;
-
打印完成后,使用405 nm蓝光(3 W)进行光交联180 s,得到不同功能的支架:
- GPP:空白GelMA-PBA/PVA双网络水凝胶支架
- BOx@GPP:负载BOx纳米颗粒的GPP支架
- MMBOx@GPP:负载MMBOx纳米颗粒的GPP支架
- MMBOx/Rapa@GPP:共负载MMBOx与雷帕霉素的GPP支架
二、材料的理化与催化性能表征
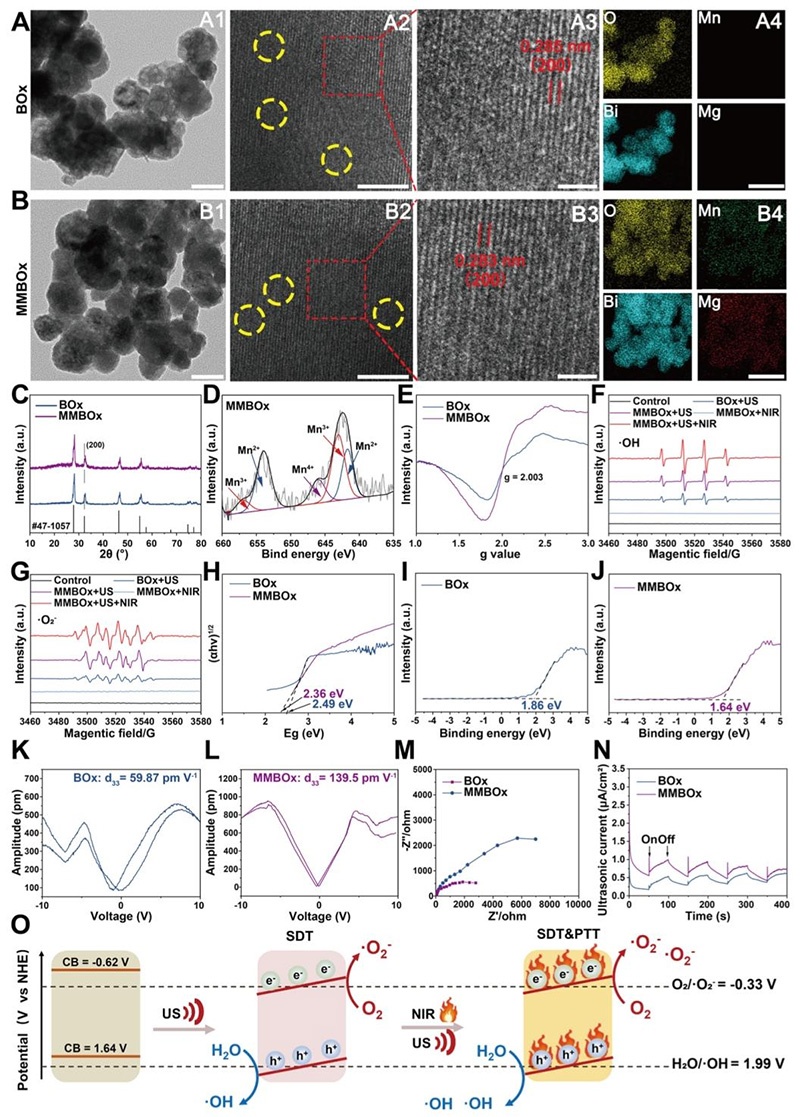
- 结构与电子特性表征:通过TEM、HRTEM、HAADF-STEM、XRD、XPS、EPR等技术,证实MMBOx纳米颗粒粒径约50 nm,Mg/Mn元素均匀掺杂,氧空位浓度从BOx的49.53%提升至63.1%;掺杂导致晶格畸变,压电系数d₃₃从59.87 pm/V提升至139.5 pm/V,压电性能显著增强。
- 光热与声动力性能:808 nm近红外(NIR)激光照射下,MMBOx展现出优异的光热转换效率,干湿环境下均有稳定的升温性能,5次激光开/关循环后光热性能无明显衰减;超声(US)照射下可高效产生·OH和·O₂⁻活性氧,NIR+US联合照射时,光热效应可进一步放大ROS生成效率。
-
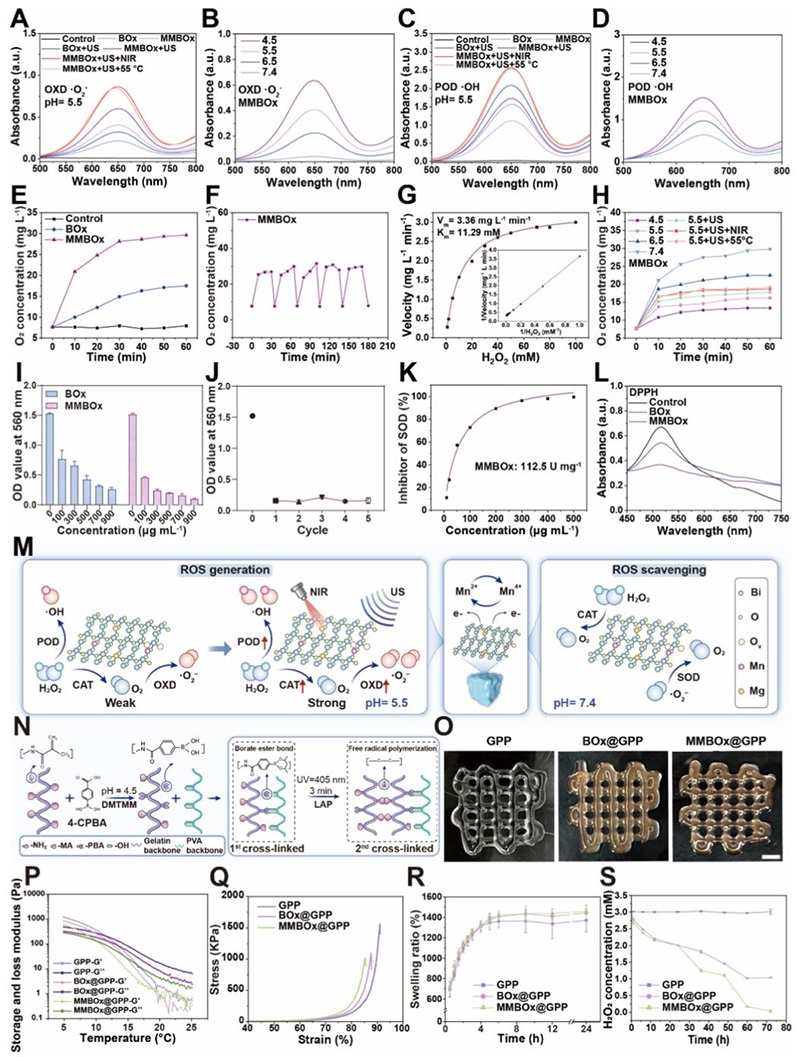
pH逻辑门控多酶样活性:
- 酸性环境(pH 4.5-6.28,对应感染微环境):MMBOx主要表现出POD、OXD样活性,pH越低活性越强,US+NIR照射可进一步放大活性,实现按需ROS生成用于杀菌;
- 中性/弱酸性环境(pH>6.28,对应组织修复微环境):MMBOx主要表现出CAT、SOD样活性,高效清除过量ROS,恢复氧化还原稳态;
- MMBOx的SOD样活性达112.5 U/mg,且多轮催化循环后仍保持稳定的活性。
三、体外抗菌性能实验
实验菌株
革兰氏阳性菌:金黄色葡萄球菌(S. aureus,ATCC 29213);革兰氏阴性菌:大肠杆菌(E. coli,ATCC 25922)
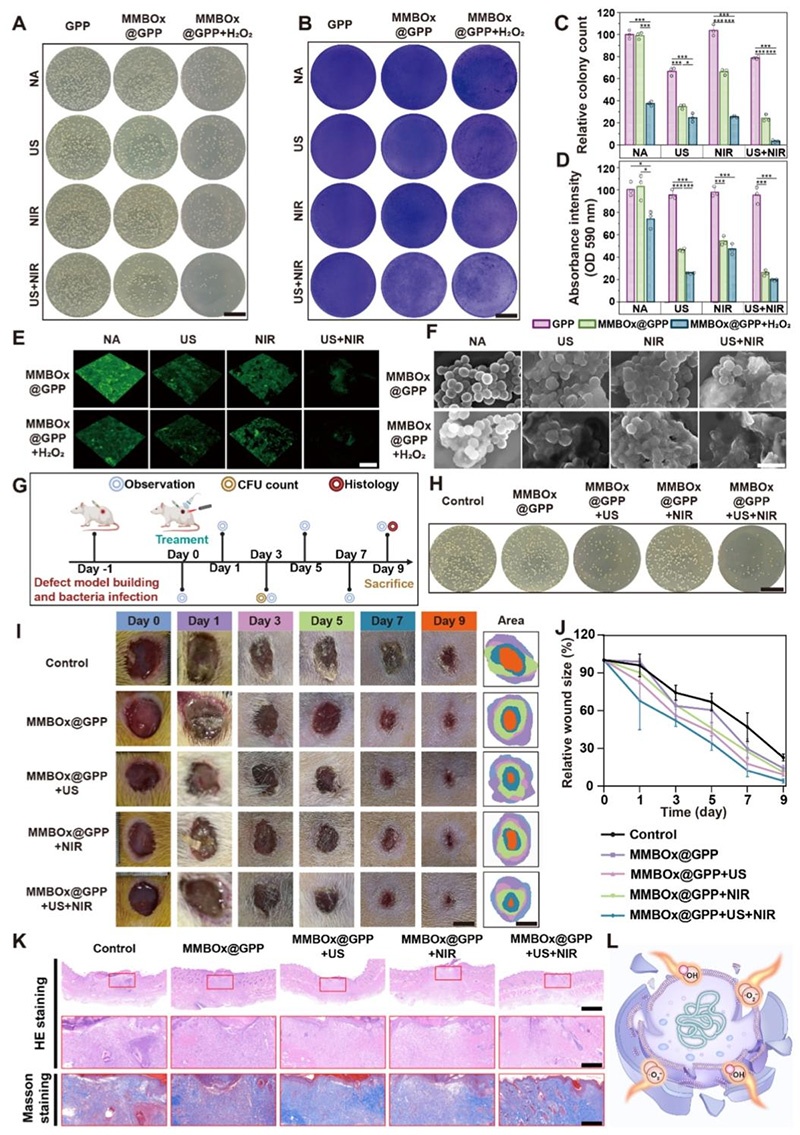
浮游菌杀菌实验
- 将3D打印水凝胶支架浸入含100 μM H₂O₂的细菌悬液中,施加外场干预(US:1.5 W/cm²,1 MHz,50%占空比,10 min;NIR:808 nm,1.4 W/cm²,10 min);
- 干预结束后,取20 μL处理后的菌液涂布于LB琼脂平板,37℃恒温培养24 h;
- 对平板菌落拍照,通过ImageJ软件进行菌落计数,计算杀菌率。
生物膜清除实验
- 将菌液接种于LB培养基,37℃静置培养12 h形成成熟细菌生物膜,PBS洗涤去除浮游菌;
- 加入不同支架并施加对应的外场干预,继续培养12 h;
- 通过结晶紫染色、活/死细菌染色评估生物膜破坏效果,乙醇洗脱结晶紫后检测590 nm处吸光度,定量生物膜生物量;
- 通过SEM观察处理后细菌的形态结构变化。
四、体外抗衰与成骨性能实验
细胞模型构建
提取4周龄SD大鼠的骨髓间充质干细胞(BMSCs),使用100 μM H₂O₂刺激3天,构建细胞衰老模型。
核心实验内容与步骤
- 细胞相容性测试:将BMSCs与不同浓度纳米颗粒/复合水凝胶共培养,通过CCK-8法检测培养第1、4、7天的细胞活力,钙黄绿素-AM/PI活/死染色观察细胞存活状态。
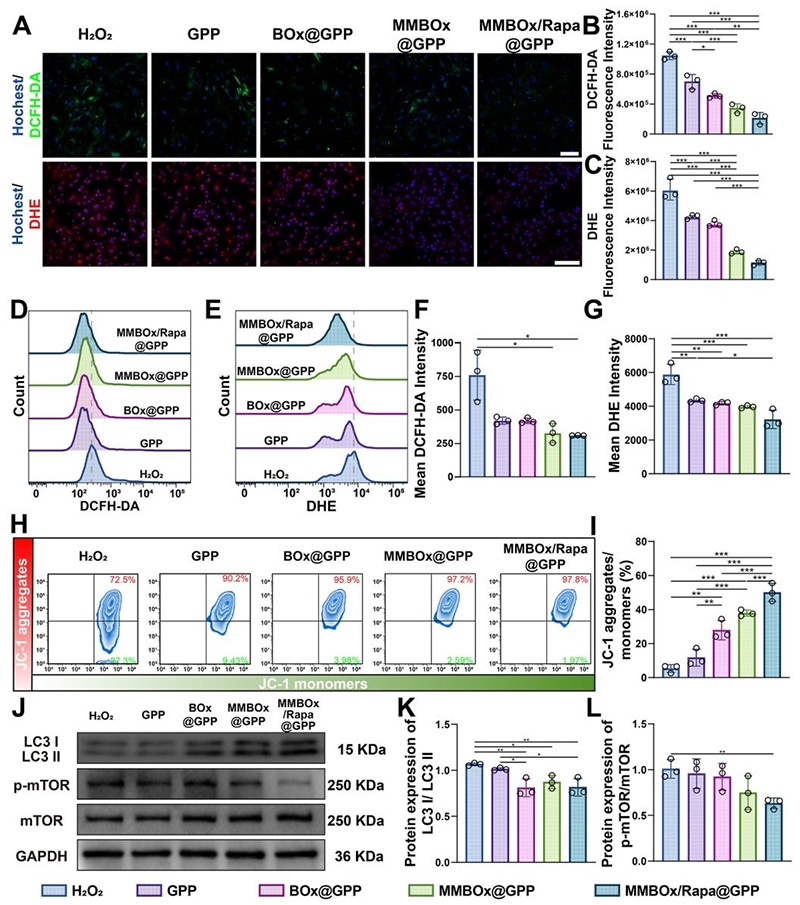
- 胞内ROS与线粒体功能检测:使用DCFH-DA/DHE荧光探针染色,结合共聚焦激光扫描显微镜与流式细胞术,定量检测胞内ROS与超氧阴离子水平;通过JC-1染色结合流式细胞术,检测线粒体膜电位变化。
- 自噬水平检测:通过Western blot技术,检测自噬相关蛋白LC3 I/II、p-mTOR、mTOR的表达水平,分析细胞自噬激活情况。
-
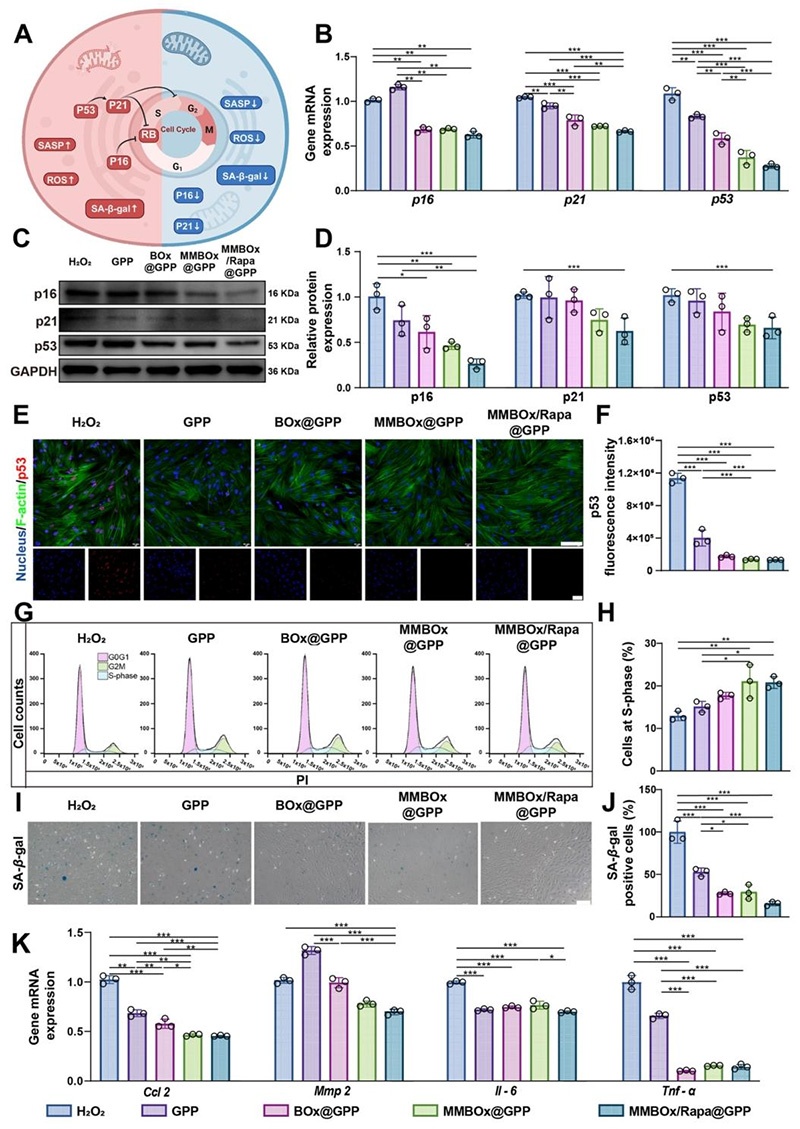
细胞衰老表型检测:
- SA-β-半乳糖苷酶染色,统计衰老阳性细胞比例;
- qRT-PCR检测衰老相关基因(p16、p21、p53)与SASP相关基因(Ccl2、Mmp2、Il-6、Tnf-α)的mRNA表达;
- Western blot检测衰老相关蛋白的表达水平;
- PI染色结合流式细胞术,分析细胞周期分布变化。
-
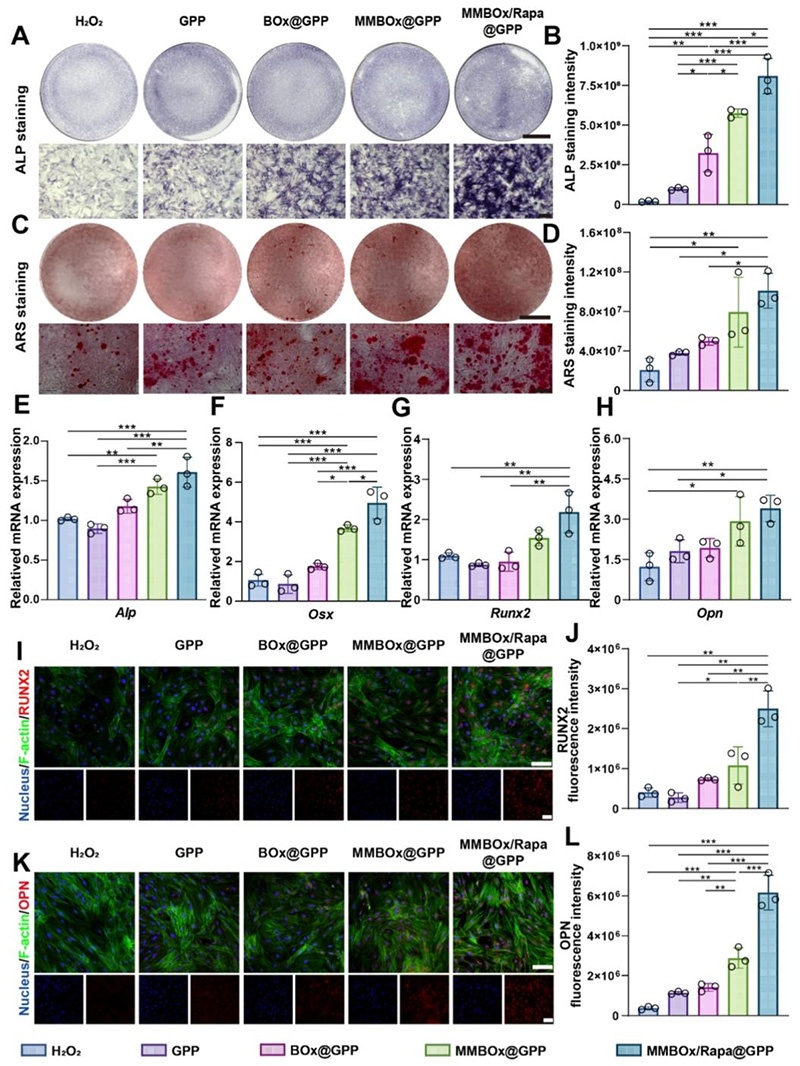
成骨分化能力检测:
- 将BMSCs与治疗平台共培养于成骨诱导培养基中,第7天进行碱性磷酸酶(ALP)染色与活性定量检测;
- 第21天进行茜素红S(ARS)染色,检测矿化结节形成情况并定量;
- qRT-PCR检测成骨相关基因(Alp、Osx、Runx2、Opn)的mRNA表达;
- 免疫荧光染色检测RUNX2、OPN成骨相关蛋白的表达水平。
五、分子机制探究
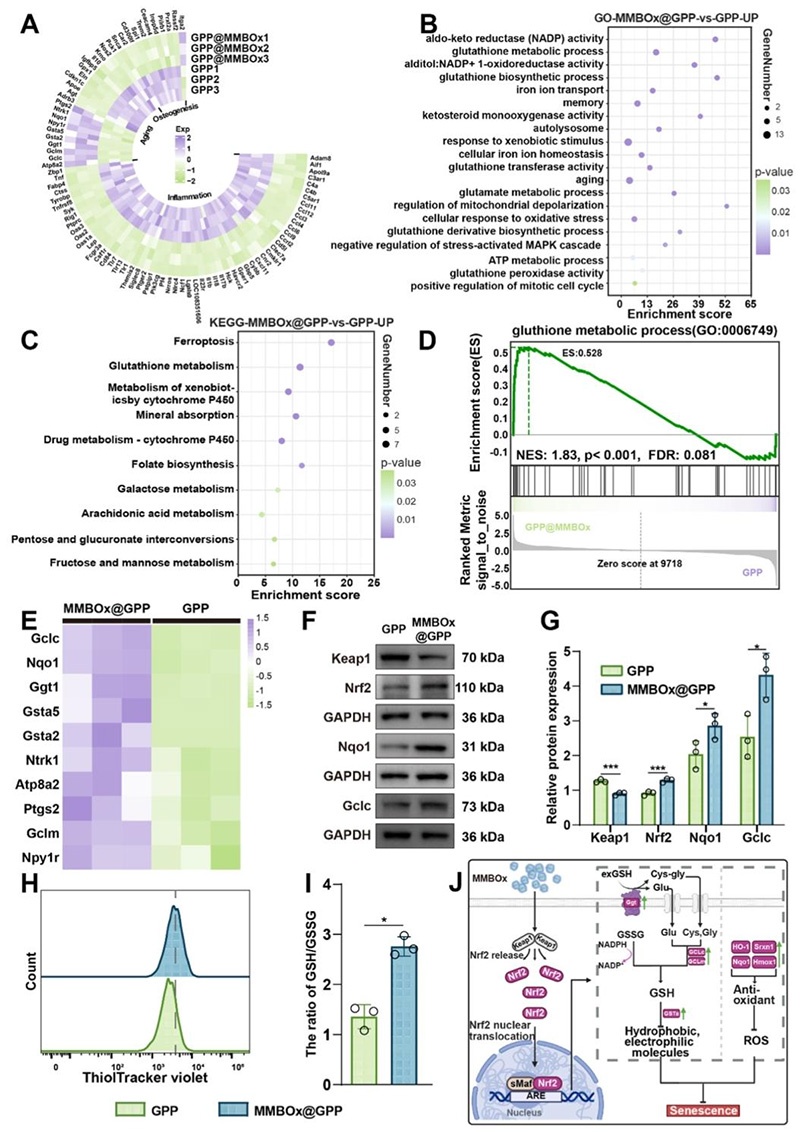
- RNA测序(RNA-seq)分析:对GPP与MMBOx@GPP处理的衰老BMSCs进行转录组测序,筛选差异表达基因(DEGs),通过GO、KEGG、GSEA富集分析,PPI蛋白互作网络分析,挖掘核心调控通路。
- 关键通路验证:通过qRT-PCR、Western blot技术,验证Keap1-Nrf2信号通路、谷胱甘肽(GSH)代谢通路关键基因与蛋白的表达水平。
- GSH含量与氧化还原状态检测:通过ThiolTracker Violet染色结合流式细胞术检测胞内GSH含量,使用GSH/GSSG检测试剂盒定量胞内GSH/GSSG比值。
- GSH耗竭验证实验:使用GSH合成抑制剂丁硫氨酸亚砜胺(BSO)处理细胞,耗竭胞内GSH,验证GSH代谢在MMBOx介导的细胞抗衰中的核心作用。
六、体内动物实验
1. 体内抗菌与创面愈合实验
- 动物模型:8周龄SD大鼠背部全层皮肤缺损感染模型(缺损尺寸10 mm×10 mm,接种10⁶ CFU S. aureus)
- 实验步骤:感染12 h后,将不同水凝胶平台植入缺损部位,施加对应的外场干预;第3天处死大鼠,取创面组织匀浆进行菌落计数;每2天拍照记录创面愈合情况,计算创面闭合率;第9天处死大鼠,取创面组织进行H&E、Masson染色组织学分析。
2. 老年骨缺损修复体内实验
- 动物模型:20月龄自然衰老雄性SD大鼠,颅骨临界尺寸缺损模型(双侧对称制备直径5 mm的圆形骨缺损)
-
实验步骤:
- 骨缺损处分别植入GPP、MMBOx@GPP、MMBOx/Rapa@GPP支架,未处理缺损作为对照组;
- 术后1周处死大鼠,取颅骨标本,通过免疫荧光染色检测局部衰老、氧化应激、炎症相关标志物的表达;
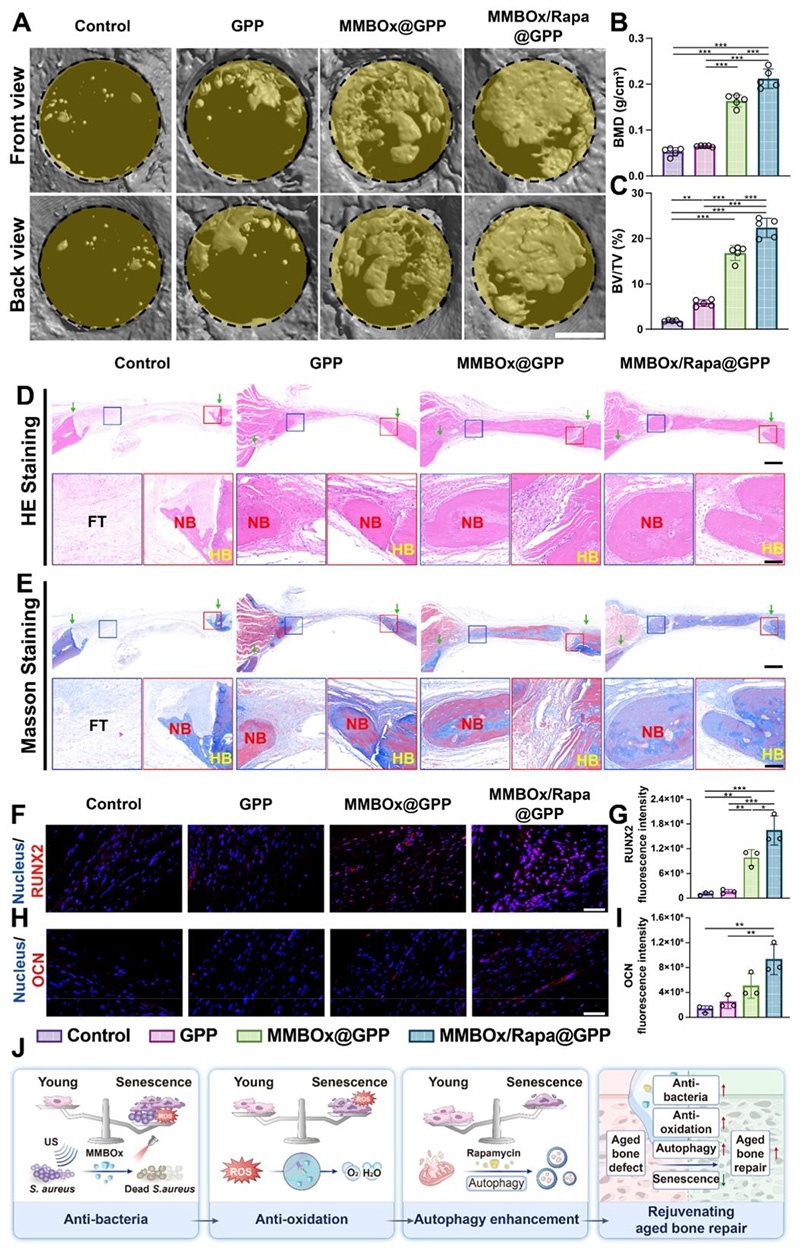
- 术后12周处死大鼠,取颅骨标本,通过micro-CT扫描与三维重建,定量分析骨体积分数(BV/TV)、骨矿物质密度(BMD)等骨再生指标;
- 通过H&E、Masson三色染色进行组织学分析,免疫荧光染色检测成骨、血管生成、巨噬细胞极化相关标志物;
- 取大鼠心、肝、脾、肺、肾主要脏器进行H&E染色,评估支架的体内长期生物安全性。