

重症骨缺损是骨科领域最具挑战性的疾病之一,自体骨移植是目前骨再生的金标准,但存在供体短缺、移植物质量不均等局限性。骨髓(BM)因富含骨髓间充质干细胞(BMSCs)和多种生长因子,能提供最优的再生微环境,常与自体骨联合用于临床骨缺损修复,但其在治疗临界骨缺损时仍存在明显不足。
骨髓发挥修复作用的核心局限主要体现在三方面:一是骨髓抽吸物中BMSCs浓度极低(仅0.001%~0.02%),无法为临界骨缺损再生提供足够的干细胞;二是骨髓基质力学性能差,需结合自体骨或脱矿骨基质才能保证力学稳定性;三是骨髓基质降解过快,导致生长因子释放与骨再生的时间进程不匹配,无法持续提供成骨信号。
现有研究虽尝试将BMSCs与生物材料支架结合,但对骨再生的动态微环境模拟不足,且缺乏针对骨修复的成骨微环境特异性工程化设计。因此,借鉴骨髓的再生特性,构建能模拟骨髓功能、实现治疗因子时序释放的骨髓模拟微环境,成为解决临界骨缺损修复的关键研究方向。
水凝胶微球因力学性能可调、可注射性好、能模拟天然细胞微环境,成为时序控释生长因子、重构干细胞微环境的理想载体,为骨髓模拟微环境的构建提供了可行的材料基础。
本研究设计了两种具有不同降解速率的杂化水凝胶微球,结合生物活性肽的时序释放特性,构建骨髓模拟微环境:①快速降解的明胶甲基丙烯酰基(GelMA)微球(GM)负载外源性BMSCs并偶联干细胞归巢肽(SKP),实现内源性BMSCs募集并增强干细胞干性;②缓慢降解的壳聚糖甲基丙烯酰基(ChitoMA)微球(CM)负载血管生成肽(KLT)和成骨肽(OGP),实现血管成熟和成骨分化的持续调控。
将两种微球通过静电作用自组装,与3D打印聚乳酸-羟基乙酸共聚物/羟基磷灰石(PLGA/HA)支架结合,形成骨组织工程复合支架,使其释放规律与骨再生的动态过程匹配:早期释放SKP和BMSCs实现干细胞募集与免疫调控,后期释放OGP和KLT实现血管生成与成骨分化,最终在大鼠股骨髁临界骨缺损模型中验证其骨再生效果。
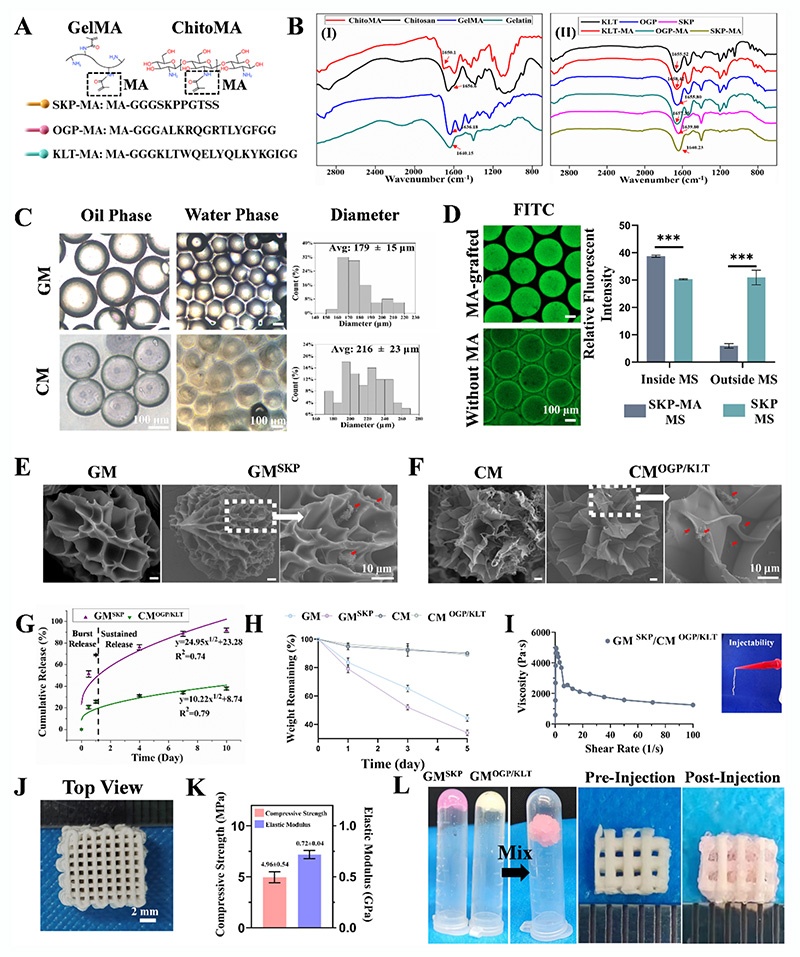
1)通过微流控芯片制备出粒径均一的GM(179±15 μm)和CM(216±23 μm)微球,傅里叶红外光谱(FTIR)和核磁共振(¹H NMR)验证了MA基团成功接枝,GelMA和ChitoMA的接枝率分别约为60%和20%,生物活性肽也成功甲基丙烯酰化;
2)荧光标记和扫描电镜(SEM)证实肽通过光交联成功偶联在微球上,无明显游离;流变学分析显示肽的引入降低了水凝胶分子网络交联度,提升了吸水率;
3)体外释放和降解实验表明,GM-SKP在10天内实现SKP近完全释放(92%),CM-OGP/KLT实现OGP/KLT的持续释放;GM在胶原酶作用下降解远快于CM,肽的引入轻微加速微球降解;
4)Zeta电位显示GM-SKP带负电、CM-OGP/KLT带正电,可通过静电作用自组装,且杂化微球具有剪切稀化特性,可注射性良好;
5)3D打印PLGA/HA支架具有相互连通的孔隙,抗压强度为4.96±0.54 MPa,弹性模量为0.72±0.04 GPa,与松质骨力学性能相当。
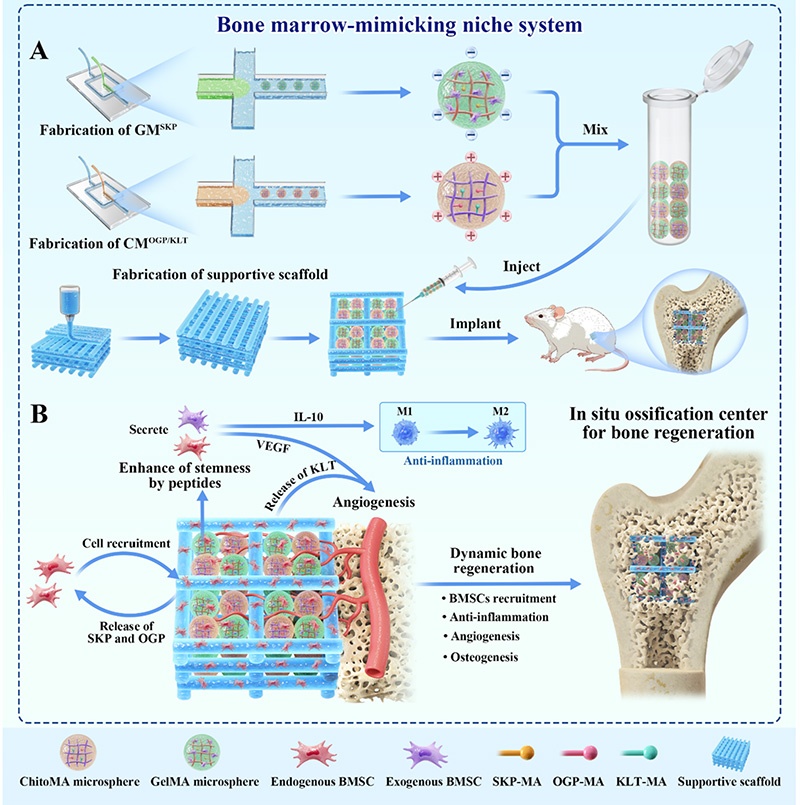
本研究通过一系列体外实验验证了骨髓模拟微环境的生物相容性、干细胞募集/干性维持、血管生成、免疫调节和成骨分化能力,核心结果如下:
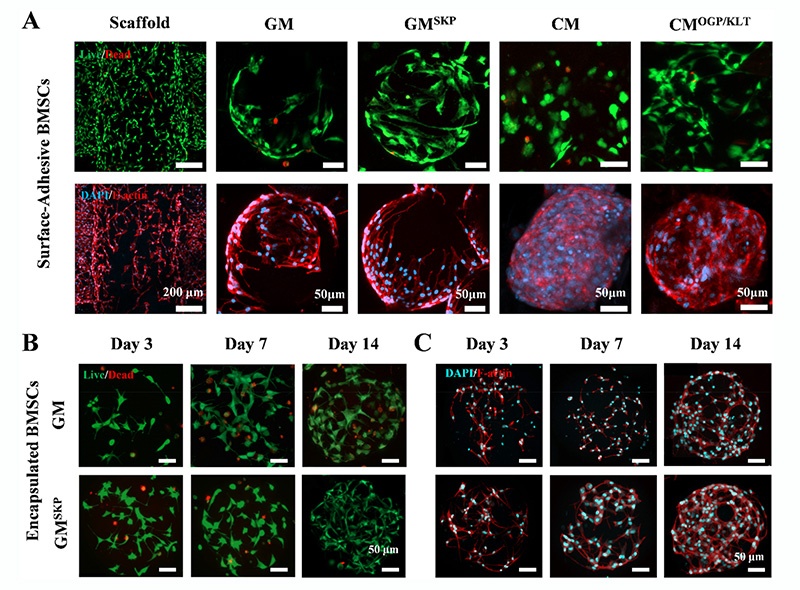
活/死染色和细胞骨架染色显示,BMSCs在所有微球和支架表面均表现出良好的粘附、铺展和活性,CM经OGP/KLT功能化后显著改善了BMSCs的铺展形态;CCK8实验表明,生物活性肽修饰的微球组BMSCs增殖率更高;微流控芯片制备的BMSCs负载微球中,干细胞存活率高且能正常增殖铺展,SKP的存在进一步增强了其铺展和增殖能力。
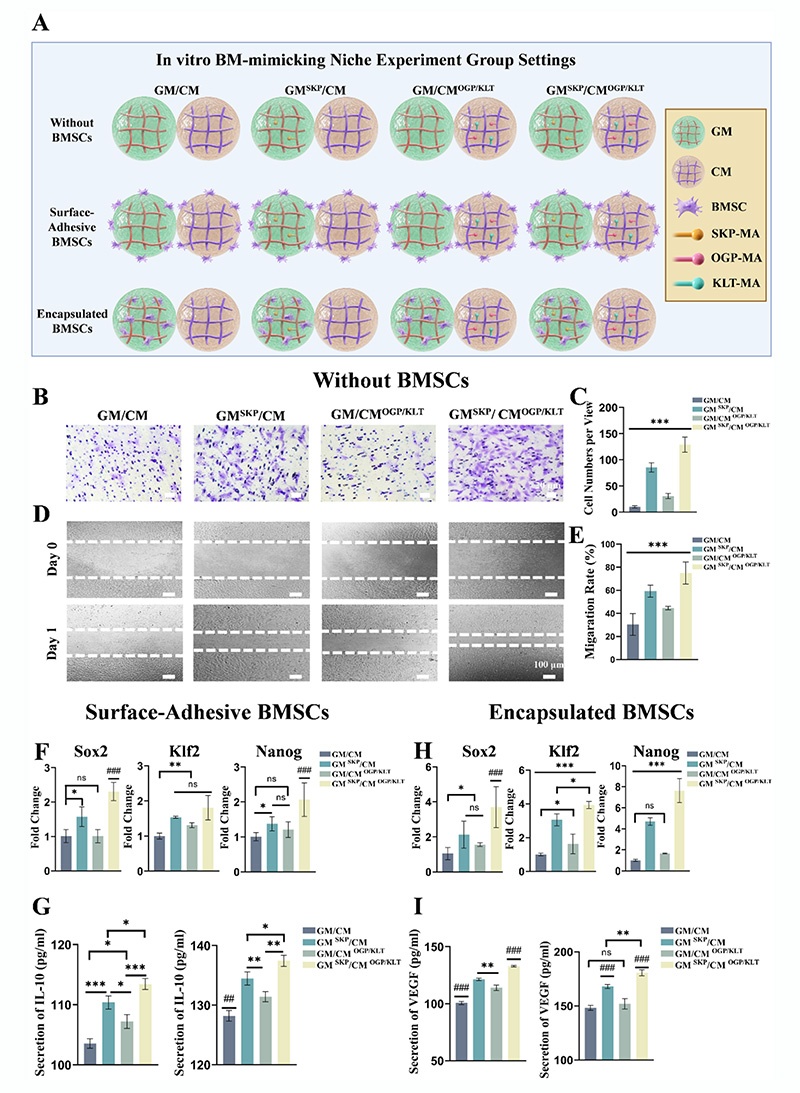
Transwell迁移和划痕实验证实,SKP和OGP/KLT均能促进BMSCs迁移,且SKP效果更显著;qRT-PCR结果显示,GM-SKP/CM-OGP/KLT组合对BMSCs干性相关基因(Sox2、Klf2、Nanog)的上调作用最显著;ELISA实验表明,肽修饰微球能显著促进BMSCs分泌VEGF和IL-10等再生因子,且3D包裹的BMSCs响应更显著。该微环境能同时募集内源性BMSCs、维持外源性BMSCs干性,为骨再生早期微环境调控奠定基础。
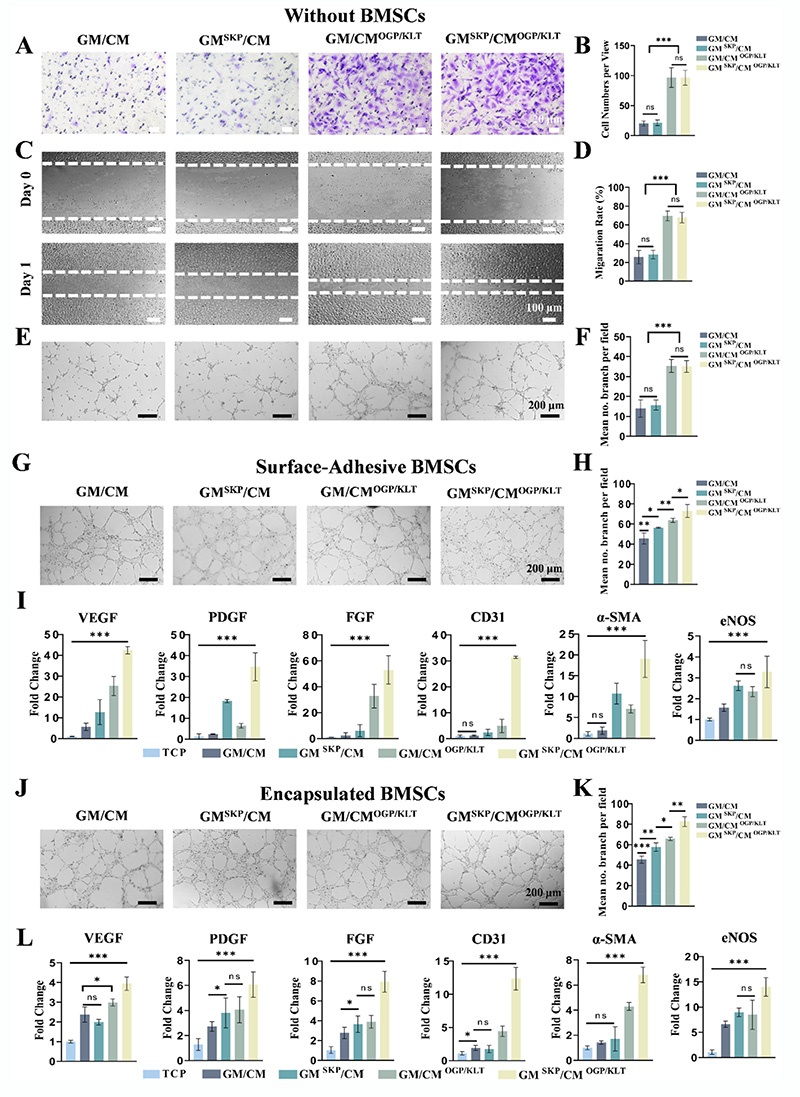
KLT是血管生成的核心肽,能显著促进人脐静脉内皮细胞(HUVECs)的增殖、迁移和管样结构形成;BMSCs的旁分泌作用与KLT协同,进一步增强血管生成能力;qRT-PCR证实,GM-SKP/CM-OGP/KLT组能显著上调HUVECs的血管生成相关基因表达,3D包裹BMSCs的旁分泌效果更显著,说明该微环境能通过肽释放和干细胞旁分泌双重途径促进血管生成。
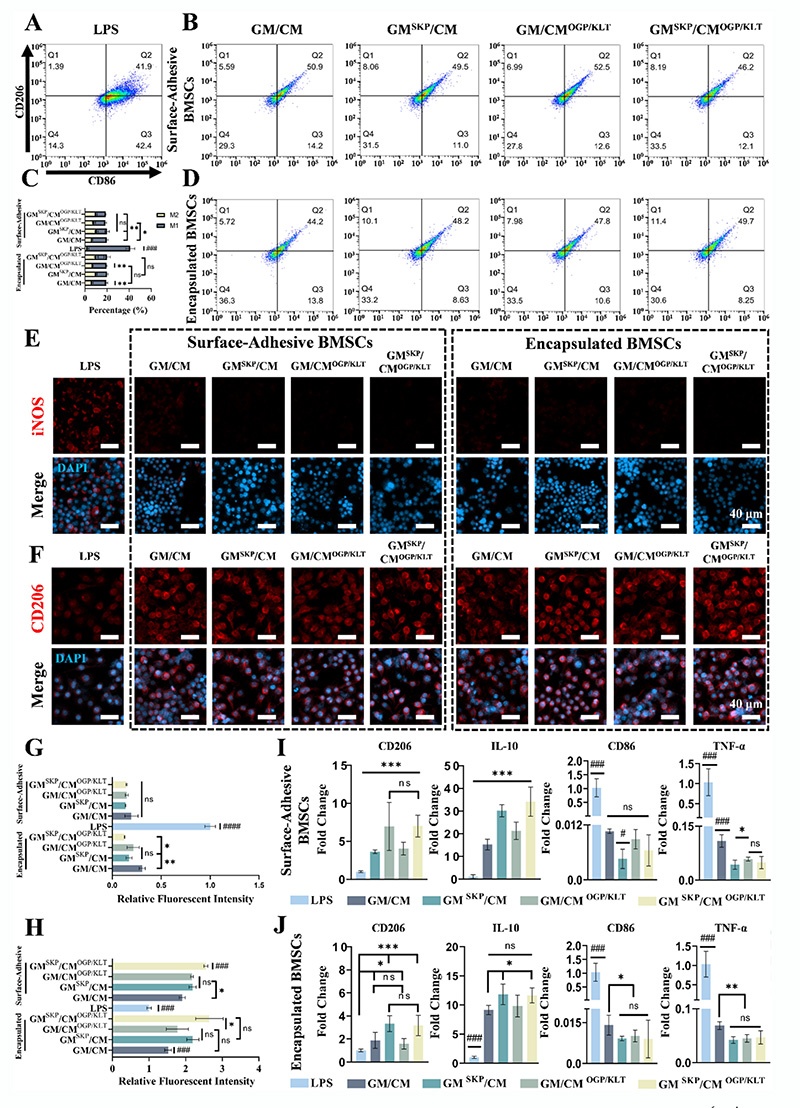
经脂多糖(LPS)激活的RAW264.7巨噬细胞在BMSCs条件培养基作用下,M1表型(促炎)标志物iNOS、CD86、TNF-α、IL-6显著下调,M2表型(抗炎)标志物CD206、IL-10显著上调;其中GM-SKP/CM-OGP/KLT组的免疫调节效果最显著,能有效将巨噬细胞从促炎表型极化为抗炎表型,缓解骨再生早期的过度炎症反应,营造利于修复的免疫微环境。
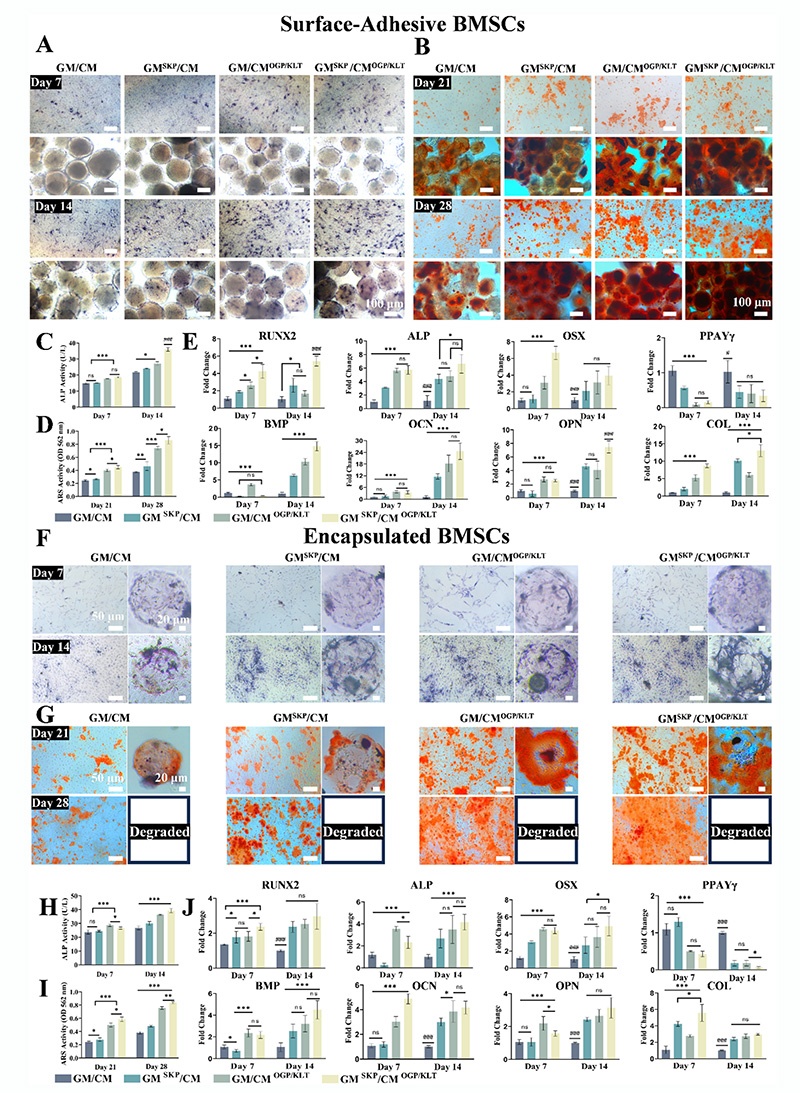
早期SKP主要维持干细胞干性,对成骨分化有轻微抑制,而OGP/KLT能显著促进BMSCs的碱性磷酸酶(ALP)活性和矿化结节形成;第14天后,SKP与OGP/KLT协同作用,显著上调成骨相关基因(RUNX2、OSX、OCN、OPN等)表达;GM-SKP/CM-OGP/KLT组合的成骨分化效果最优,且3D包裹的BMSCs成骨潜能更显著;GM在28天近完全降解,使BMSCs能与周围组织相互作用,启动原位成骨。
构建大鼠股骨髁3mm×3mm×4mm临界骨缺损模型,设置四组实验:①对照组(仅3D打印支架);②MS组(支架负载GM/CM微球,无肽);③MSP组(支架负载GM-SKP/CM-OGP/KLT微球,无外源性BMSCs);④MSPC组(支架负载GM-SKP/CM-OGP/KLT微球,负载外源性BMSCs),通过免疫组织化学、Micro-CT、组织学染色验证骨再生效果。
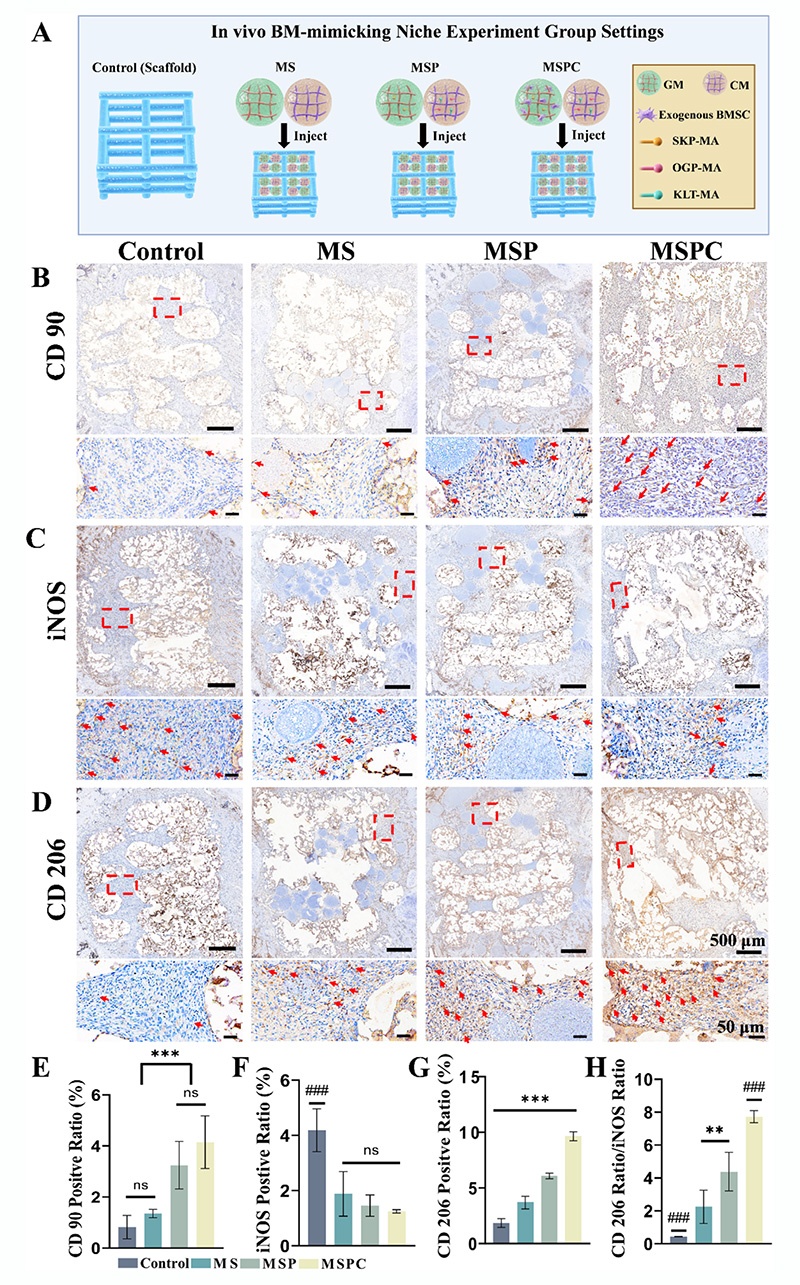
术后1周,CD90(干细胞标志物)免疫组化显示,MSPC组的干细胞募集量最多,微球为干细胞提供了额外的粘附位点;iNOS(M1)表达显著降低,CD206(M2)表达显著升高,MSPC组的CD206/iNOS比值最高,说明该骨髓模拟微环境能有效募集内/外源性干细胞,缓解早期炎症反应,为骨再生奠定基础。
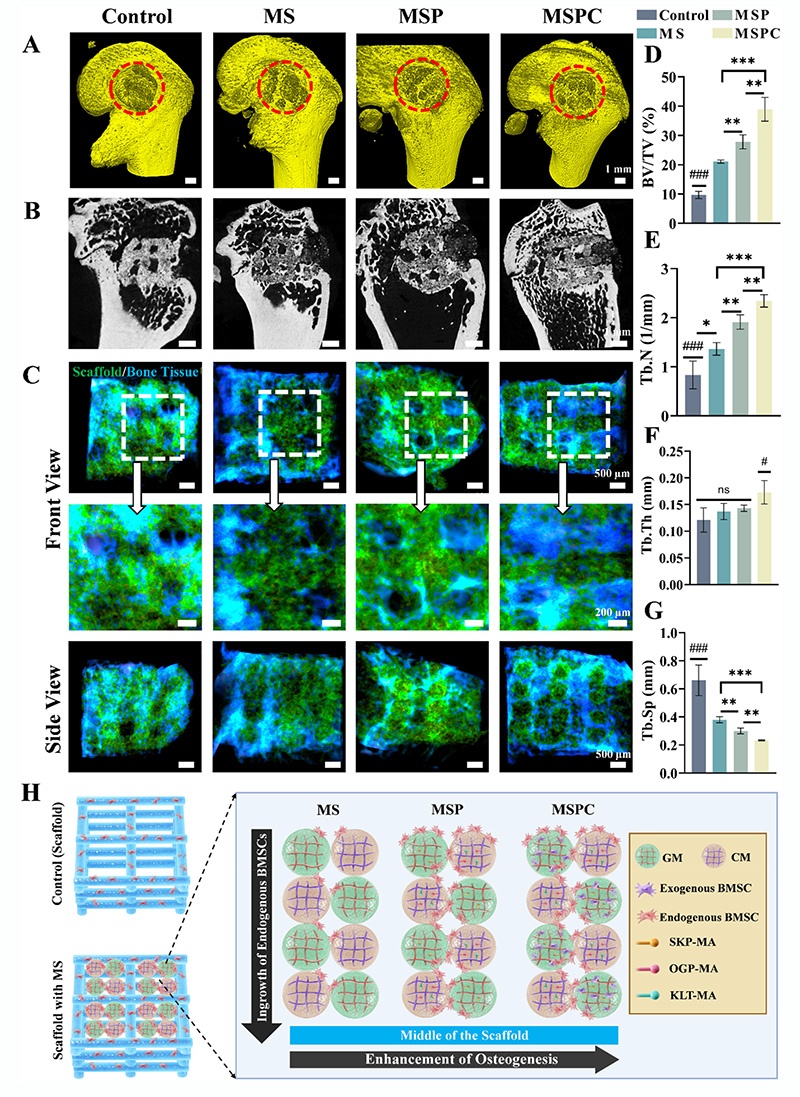
术后12周,Micro-CT结果显示:对照组几乎无新生骨形成,MS组有少量新生骨,MSP组新生骨显著增加,MSPC组支架孔隙内几乎被新生骨完全填充;定量分析显示,MSPC组的BV/TV、Tb.N、Tb.Th均为最高,Tb.Sp为最低,骨再生效果最优,证实骨髓模拟微环境能显著促进临界骨缺损的骨再生,且外源性BMSCs与内源性募集的干细胞协同作用进一步提升修复效果。
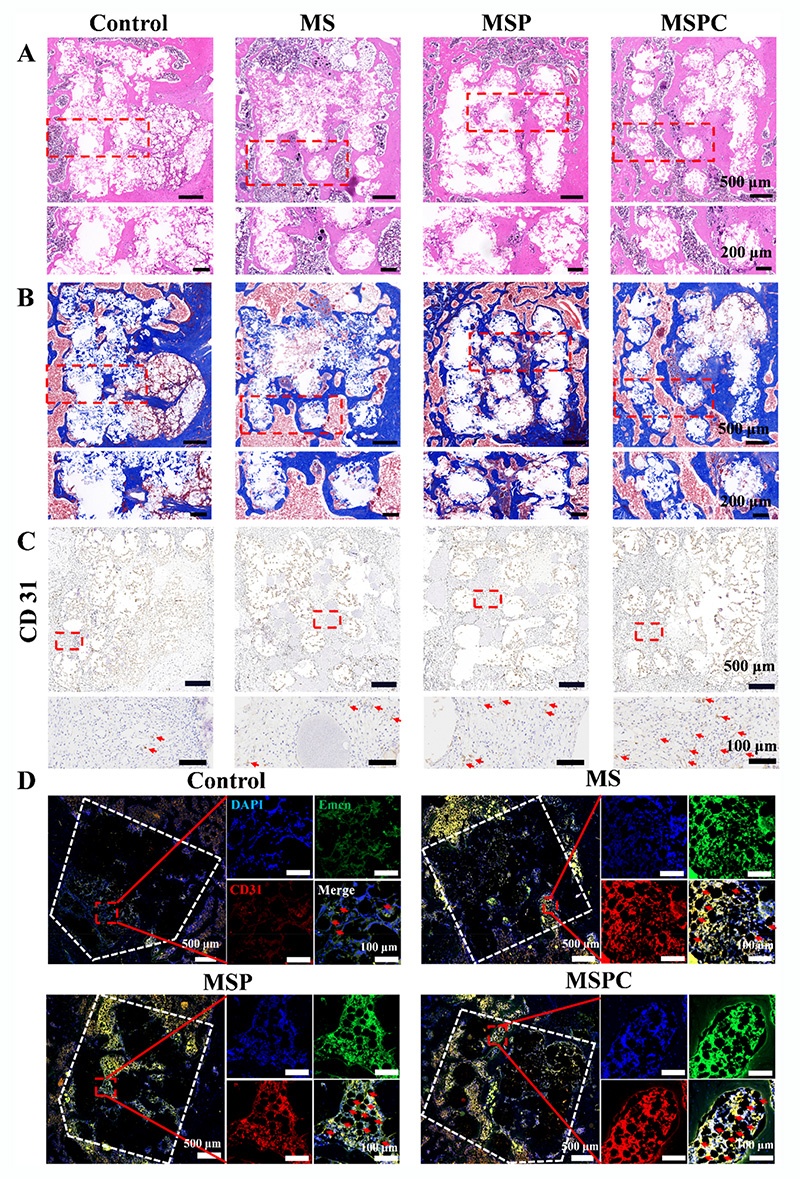
HE、Masson、Goldner三色染色显示,MSPC组的新生骨和血管网络最丰富,支架孔隙内几乎被新生骨填充;术后1周CD31免疫组化显示,MSPC组的血管密度显著高于其他组;术后12周H型血管(CD31+Emcn+,功能性成骨血管)免疫荧光显示,MSPC组的H型血管表达最广泛,证实该微环境能促进功能性血管生成,并与成骨过程协同,实现血管化骨再生。
此外,主要脏器(肝、肾、脾)的H&E染色显示,所有实验组均无组织坏死、炎症浸润等病理改变,证实该材料系统具有优异的体内生物相容性,无全身毒性。
本研究成功制备了负载BMSCs的GM-SKP快速降解释球和负载OGP/KLT的CM-OGP/KLT缓慢降解释球,两种微球通过静电作用自组装形成杂化体系,与3D打印PLGA/HA支架结合构建了骨髓模拟微环境,该体系在体外和体内实验中均表现出优异的骨再生调控能力。
该骨髓模拟微环境能精准匹配骨再生的动态过程:早期通过SKP实现内源性BMSCs募集,同时维持外源性BMSCs的干性,促进抗炎巨噬细胞极化,缓解过度炎症反应,营造利于修复的微环境;后期通过OGP/KLT的持续释放,促进功能性血管生成(包括H型血管)和BMSCs的成骨分化,最终在大鼠股骨髁临界骨缺损模型中形成原位成骨中心,显著提升骨再生效果。
该研究构建的骨髓模拟微环境结合了干细胞募集/负载、生物活性肽时序释放、免疫调节、血管生成与成骨分化的协同调控,为骨组织工程和干细胞治疗提供了新的思路和策略,有望成为临界骨缺损修复的有效方法。
本研究虽取得了良好的骨再生效果,但仍存在一定局限性,未来需进一步研究:
期刊:Bioactive Materials 54 (2025)
页码:179–200
标题:Self-assembled hybrid hydrogel microspheres create a bone marrow-mimicking niche for bone regeneration(自组装杂化水凝胶微球构建骨髓模拟微环境用于骨再生)
通讯作者:Yongwei Pan(潘永伟)、Yu Wang(王宇)、Xiumei Wang(王秀梅)
研究单位:清华大学材料科学与工程学院、首都医科大学北京友谊医院骨科、解放军总医院骨科研究所等
关键词:骨髓、骨髓间充质干细胞、水凝胶微球、生物活性肽、骨再生、生物3D打印机
全面解析森工DIW墨水直写3D打印机在该类研究中功能匹配情况及需定制功能,帮助用户更好地选择合适的3D打印设备及功能模块。
常温气动打印模块:
1.配备精密的调压模块,调压精度±1KP;
2.打印过程中可压力实时可调;
可将聚乳酸-羟基乙酸共聚物/羟基磷灰石(PLGA/HA)支架实现精准打印,制备成骨组织工程复合支架。
多通道常温气动打印:因快速降解的明胶甲基丙烯酰基(GelMA)微球(GM)和缓慢降解的壳聚糖甲基丙烯酰基(ChitoMA)微球(CM)均具备剪切稀化特性,故在打印骨组织工程复合支架的同时进行微球材料精准打印,缩短整体制备周期。
多通道常温气动打印:
1.配备精密的调压模块,调压精度±1KP;
2.对每个通道实现独立精准控压;
3.打印过程中可压力实时可调;
4.多通道打印可实现不同打印路径规划;
由于小编学识所限,文中内容难免存在疏漏或不足之处。若您发现任何错误或值得商榷的观点,恳请不吝指正,
小编将第一时间修正完善。感谢您的包容与支持!
本文内容来源于网络公开素材,发布的目的在于学术交流、研讨分享,
如相关内容涉及侵权,请联系我们,将第一时间下架内容!


森工科技AutoBio系列生物3D打印机专业版和旗舰版应用于科研场景该怎么选择?

直写式(DIW)陶瓷 3D 打印机:科研领域的材料创新利器

论文分分享 I Structure design of an innovative 3-dimensional-printed emulsion carrier for stabilizing pol

森工科技亮相第四届陶瓷增材制造前沿科学家论坛 罗建旭发表“高性能非金属材料挤出直写与粘接剂喷射工艺解决方案”主题报告

森工科技 AutoBio2000多通道食品3D打印机助力深圳大学化学与环境工程学院食品科学与工程系范方辉团队登顶食品工程 TOP 期刊

DIW直写3D打印机在陶瓷材料科研领域的应用及优势