

骨肉瘤是一种高度恶性的骨肿瘤,主要发生于儿童和青少年,好发于长骨,具有侵袭性强的特点,可造成骨破坏、剧烈疼痛、残疾甚至远处转移,临床需结合系统药物和外科手术干预。目前临床主流的保肢治疗包括肿瘤完整切除、骨缺损重建以及放化疗辅助治疗,理想状态下可同时清除肿瘤并恢复肢体功能,但骨肉瘤普遍存在的放化疗耐药性,难以实现镜下切缘阴性(R0)切除,易导致局部复发、保肢失败,往往需要二次或多次侵入性手术,严重影响患者预后。
3D打印仿生复合支架为骨肉瘤保肢治疗提供了新策略,其中羟基磷灰石(HA)、β-磷酸三钙等磷酸钙陶瓷支架因与天然骨矿物成分相似、生物相容性好、具有骨传导和骨诱导性,成为骨移植的重要替代材料。但骨肉瘤侵袭、肿瘤代谢引发的过度骨溶解及手术切除,会造成骨缺损微环境再生性差,超出支架固有修复能力;现有支架改性策略(整合生物活性因子、干细胞)虽一定程度克服该问题,却无法同时实现肿瘤杀伤与骨再生、缺乏智能微环境适应性,且材料设计复杂、再生效率不足。
骨肉瘤复发或保肢术后炎性创伤会导致缺损区H₂O₂水平显著升高、形成缺氧微环境,破坏氧化还原稳态,对内生干细胞造成持续性氧化应激,严重阻碍骨再生。理想的骨缺损修复材料需实现H₂O₂的智能催化:在肿瘤微环境中转化为高毒性活性氧(ROS)诱导肿瘤细胞凋亡,在炎性骨缺损微环境中分解为O₂缓解炎症、恢复成骨-破骨平衡。现有纳米酶类生物催化材料(金属氧化物、贵金属纳米颗粒)难以同时实现H₂O₂向ROS和O₂的智能转化,且现有治疗策略仅聚焦抗肿瘤或抗炎单一功能,尚无针对骨肉瘤保肢治疗的多效生物催化材料,因此开发可智能根除肿瘤、重塑氧化还原稳态的通用型生物催化材料成为保肢治疗的关键需求。
本研究首次设计并构建了超声激活型生物催化纳米颗粒修饰的3D打印羟基磷灰石支架(HS-ICTO),通过TiO₂纳米材料为半导体基底,构建Ti-O-Ir电子耦合结构的Ir簇(ICTO),实现H₂O₂的时空可控催化,在骨肉瘤微环境中高效生成ROS杀伤肿瘤,在骨缺损微环境中分解H₂O₂生成O₂促进骨再生,完成“肿瘤根除-骨缺损修复”的智能序贯治疗,同时验证了该支架的体外抗肿瘤、抗氧化应激、抑制破骨形成及体内肿瘤清除、骨缺损重建效果,并阐明了其催化机制。
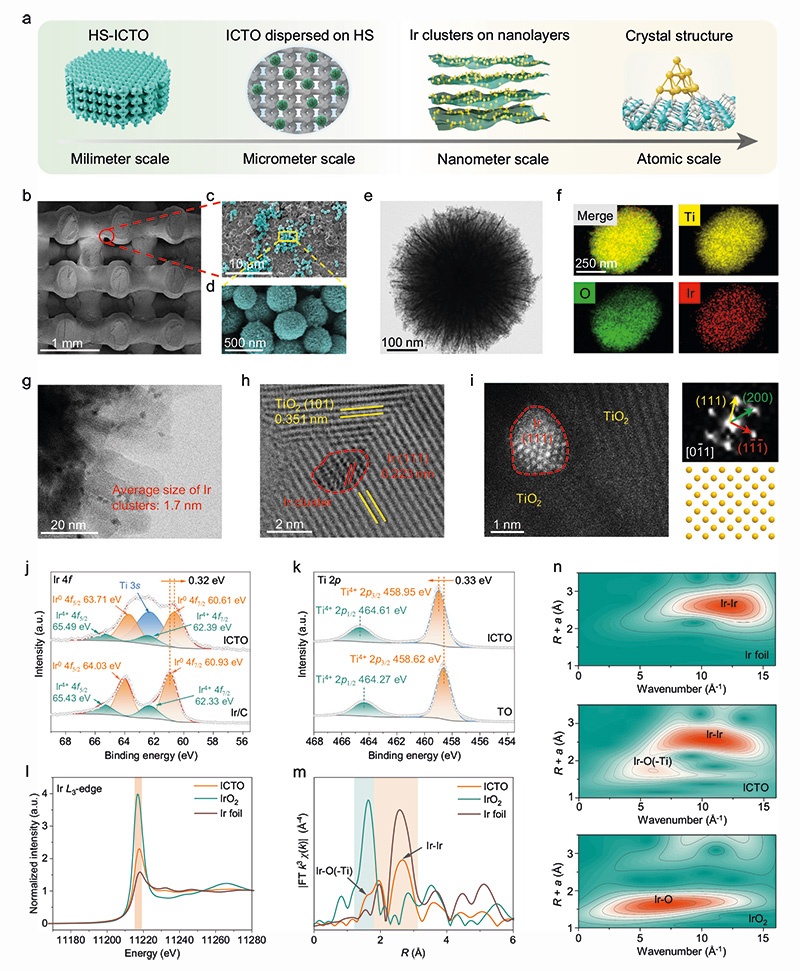
采用湿蒸发沉积法将ICTO纳米颗粒负载于3D打印HA支架(HS)表面,制备不同ICTO浓度的HS-ICTO-x支架(x=0、0.5、1.0、2.0 mg/mL)。通过场发射扫描电镜(FESEM)、能谱仪(EDS)、X射线衍射(XRD)、透射电镜(TEM)、X射线光电子能谱(XPS)、X射线吸收光谱(XAS)等手段表征支架结构,结果显示:ICTO以平均1.7 nm的Ir簇高度分散于TiO₂表面,形成Ti-O-Ir强化学耦合和界面电荷转移;HS-ICTO保留了HS的互锁交织多孔结构,Ti、Ir、Ca、P、O元素均匀分布,且ICTO负载未改变HS的力学性能(抗压强度2.02±0.15 MPa),与人体松质骨相当,ICTO纳米颗粒在支架表面稳定性好,仅在机械刮擦或外部能量干扰下发生脱落。
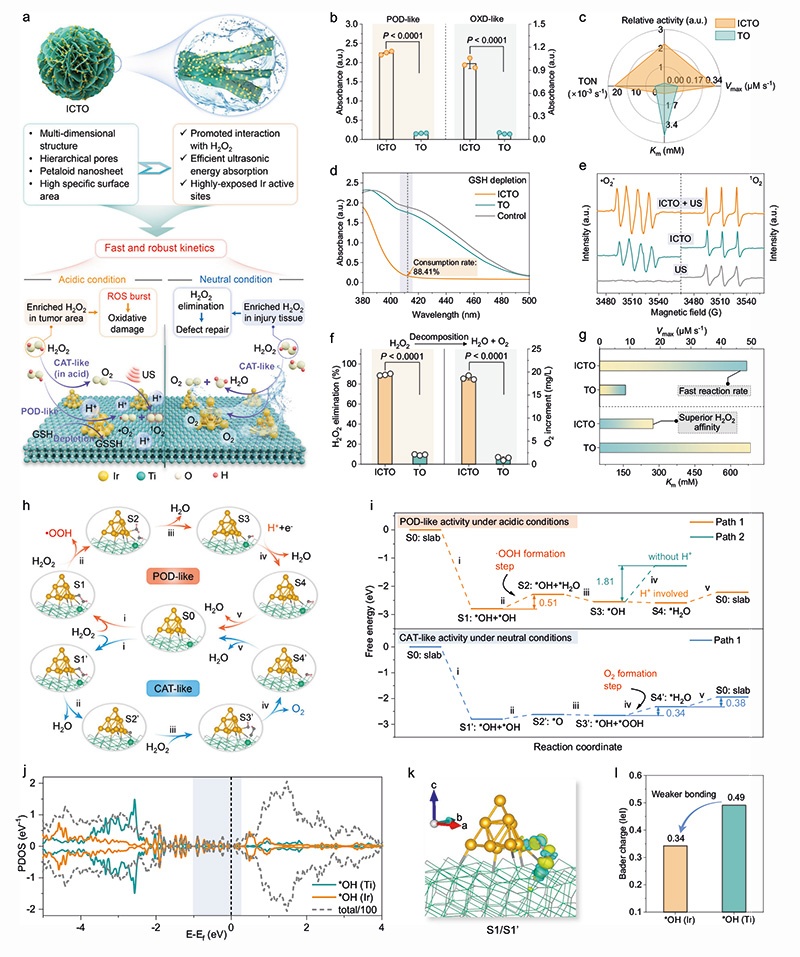
ICTO因分级花瓣状纳米片结构、高比表面积,实现了H₂O₂底物高可及性和超声能量高效吸收,具有**过氧化物酶(POD)、氧化酶(OXD)、过氧化氢酶(CAT)样三重酶活性**,且催化活性具有pH依赖性:
通过密度泛函理论(DFT)计算阐明催化机制:Ti-O-Ir界面的电子转移是多酶活性的核心,Ti位点优化氧中间体吸附,Ir位点为活性中心;POD样反应的决速步为·OOH形成(能垒0.51 eV),需酸性环境提供H+,而CAT样反应的决速步为O₂和H₂O解吸(能垒0.34/0.38 eV),在中性条件下可自发进行;Ir-OH的电子态更活跃,与H₂O₂的反应性高于Ti-OH,实现了H₂O₂的pH响应性智能催化。
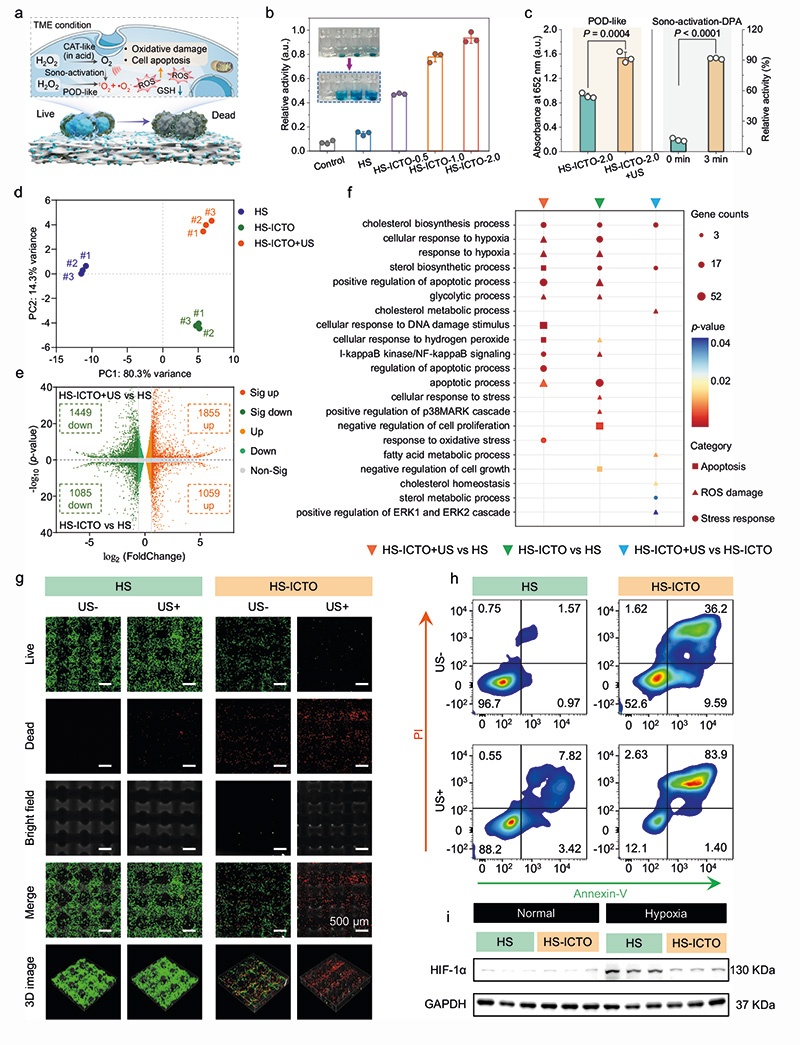
体外细胞实验以143b人骨肉瘤细胞、大鼠骨髓间充质干细胞(BMSCs)为模型,验证HS-ICTO的生物相容性和抗肿瘤活性:
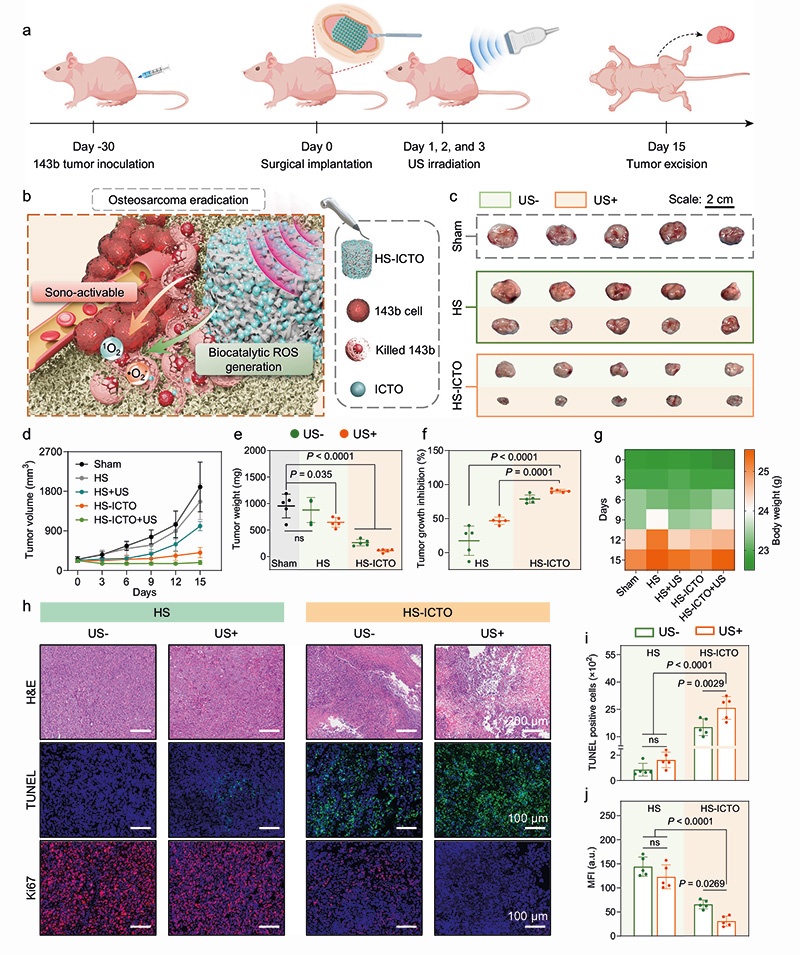
构建143b骨肉瘤裸鼠皮下移植瘤模型,将HS、HS-ICTO支架植入肿瘤组织,术后24/48/72 h给予局部超声照射(2.5 W/cm²,1 MHz,30%占空比,5 min),结果显示:
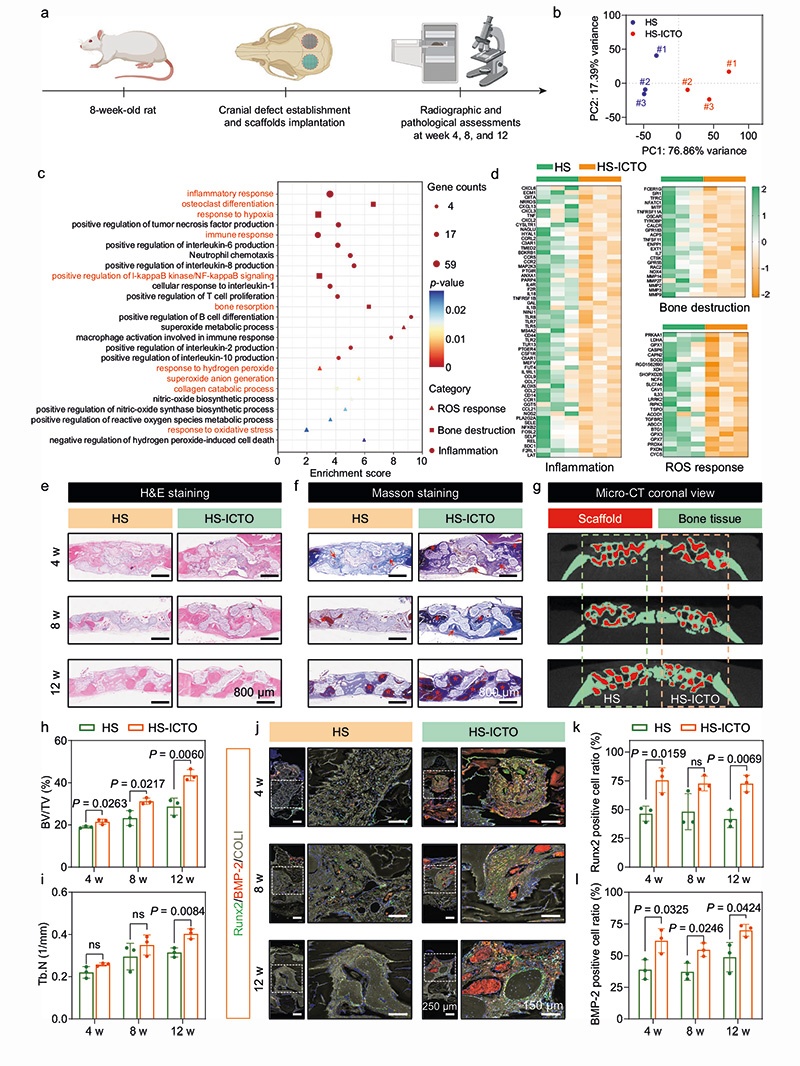
以H₂O₂诱导的BMSCs氧化应激模型验证HS-ICTO对骨再生相关干细胞的保护作用,结果显示:
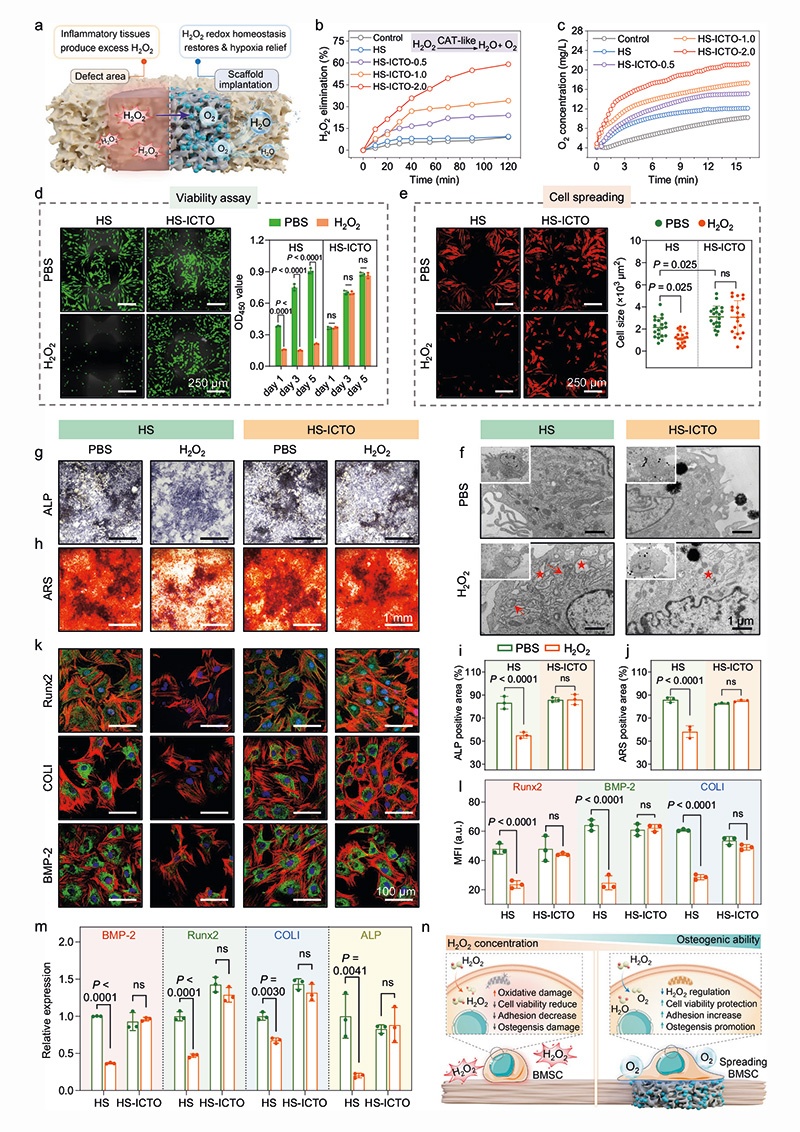
骨肉瘤相关骨破坏与破骨细胞过度活化相关,以K7M2小鼠骨肉瘤细胞与RAW264.7小鼠巨噬细胞共培养模型、RANKL诱导的RAW264.7破骨分化模型验证HS-ICTO的抗破骨效果:
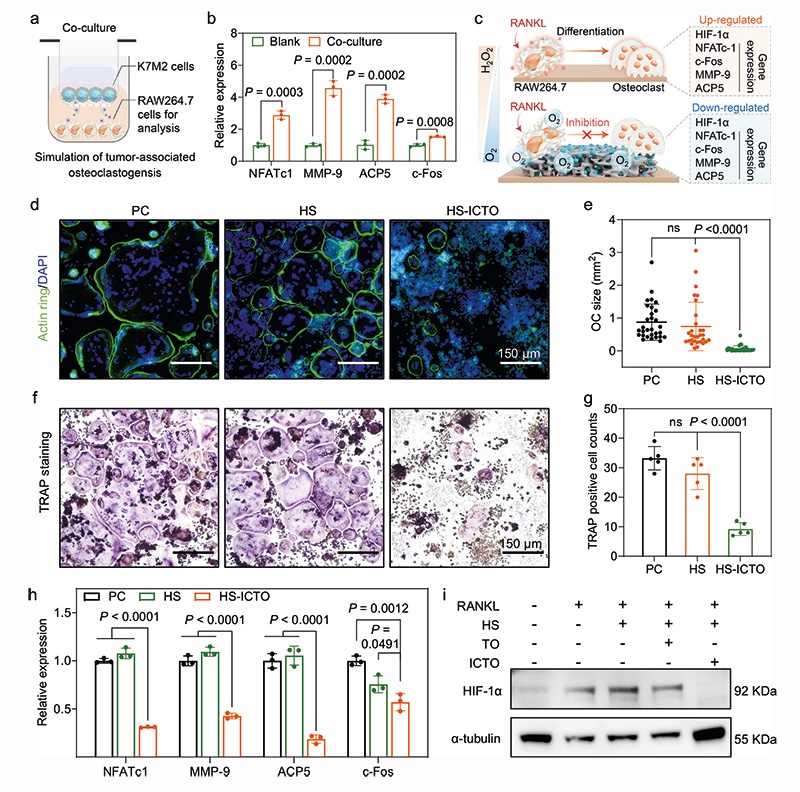
构建大鼠颅骨缺损模型(φ=5 mm),左侧植入HS、右侧植入HS-ICTO,分别在4/8/12周进行影像学和组织学检测,结果显示:
本研究成功设计并l利用直写生物3D打印机制备了超声激活与生物催化3D打印羟基磷灰石支架(HS-ICTO),该支架基于氧化还原医学理念,以H₂O₂为共同治疗靶点,实现了骨肉瘤根除和骨缺损再生的智能序贯治疗,核心结论如下:
研究同时指出,未来将进一步探索HS-ICTO的长期生物相容性,在原位骨肉瘤模型和大型动物骨缺损模型中验证其疗效,结合高强度聚焦超声等临床技术,推动其临床转化,实现术后肿瘤复发的定期局部超声激活清除,减少全身毒性和不良反应。
发表期刊:Nature Communications
DOI:https://doi.org/10.1038/s41467-025-61377-x
第一作者:Rong Xiao、Sutong Xiao(共同一作)
通讯作者:Boqing Zhang、Li Qiu、Chong Cheng
研究单位:四川大学华西医院、四川大学高分子科学与工程学院、四川大学生物医学工程学院等
核心关键词:骨肉瘤、3D打印羟基磷灰石支架、超声激活、生物催化、纳米酶、骨缺损再生、序贯治疗
全面解析森工DIW墨水直写3D打印机在该类研究中功能匹配情况及需定制功能,帮助用户更好地选择合适的3D打印设备及功能模块。
由于小编学识所限,文中内容难免存在疏漏或不足之处。若您发现任何错误或值得商榷的观点,恳请不吝指正,
小编将第一时间修正完善。感谢您的包容与支持!
本文内容来源于网络公开素材,发布的目的在于学术交流、研讨分享,
如相关内容涉及侵权,请联系我们,将第一时间下架内容!


森工科技AutoBio系列生物3D打印机专业版和旗舰版应用于科研场景该怎么选择?

直写式(DIW)陶瓷 3D 打印机:科研领域的材料创新利器

论文分分享 I Structure design of an innovative 3-dimensional-printed emulsion carrier for stabilizing pol

森工科技亮相第四届陶瓷增材制造前沿科学家论坛 罗建旭发表“高性能非金属材料挤出直写与粘接剂喷射工艺解决方案”主题报告

森工科技 AutoBio2000多通道食品3D打印机助力深圳大学化学与环境工程学院食品科学与工程系范方辉团队登顶食品工程 TOP 期刊

DIW直写3D打印机在陶瓷材料科研领域的应用及优势