二、研究内容
2.1 材料与方法
(1)实验材料
- 羟基磷灰石(HAp):粉末状,平均粒径<1 μm,分子量502.31 g/mol(Acros Organics,美国);
- 海藻酸钠(SA):低黏度粉末,平均分子量427 kDa(Sigma–Aldrich,意大利米兰);
- 胶原肽:鱼源(Coll₆)与牛源(Collᵦ),粉末状,平均分子量2 kDa(Lapi Gelatine S.p.A.,意大利);
- 细胞与试剂:人真皮成纤维细胞(HDFs)、DMEM培养基、青霉素/链霉素、BCA蛋白定量试剂盒等(Merck、GIBCO等品牌)。
(2)生物墨水制备
制备两种生物墨水(HAp/SA/Coll₆、HAp/SA/Collᵦ),三者质量比为5.5:10:10:① 将10%(w/v)胶原肽(Coll₆或Collᵦ)溶于蒸馏水,60℃搅拌30 min;② 加入10%(w/v)HAp,充分分散;③ 加入5.5%(w/v)SA,60℃持续搅拌1 h,室温温和搅拌过夜至均一。
(3)表征与测试方法
- FTIR分析:采用Agilent Cary 630 FTIR光谱仪(ATR模式),4000–500 cm⁻¹波数范围,分辨率4 cm⁻¹,分析胶原肽化学结构;
- 流变学表征:使用MCR 92流变仪(25 mm平行板,间隙50 μm),测试频率0.05–100 Hz下的黏度(η)、储能模量(G')、损耗模量(G'')与剪切应力(τ);
- 3D打印:采用DIW墨水直写生物3D打印机,27 G锥形喷嘴,气动挤出;打印参数见表4,打印后用1%(w/v)CaCl₂溶液交联10 min;
- 可打印性评估:① 细丝融合测试:打印单层平行细丝(间距1.4–1.8 mm),ImageJ测量细丝融合长度(fₛ)、厚度(fₜ)、间距(f_d);② 宏观多孔结构(20×20×0.6 mm³方格):计算可打印性(Pᵣ)、扩散率(Dᵣ)、收缩率(S);
- 凝胶分数分析:打印10×10×1 mm³样品,交联后干燥称重(W₀),蒸馏水浸泡24 h后再次干燥称重(W_f),凝胶分数=(W_f/W₀)×100%;BCA法定量释放的胶原肽;
- 溶胀测试:样品交联后称重(Wᵢ),37℃ PBS中浸泡48 h,不同时间点称重(Wₛ),溶胀率=(Wₛ–Wᵢ)/Wᵢ×100%;
- 细胞相容性评估:间接细胞毒性测试(刃天青代谢法),检测HDFs在生物墨水浸提液中的代谢活性。
2.2 结果与分析
(1)胶原肽FTIR分析
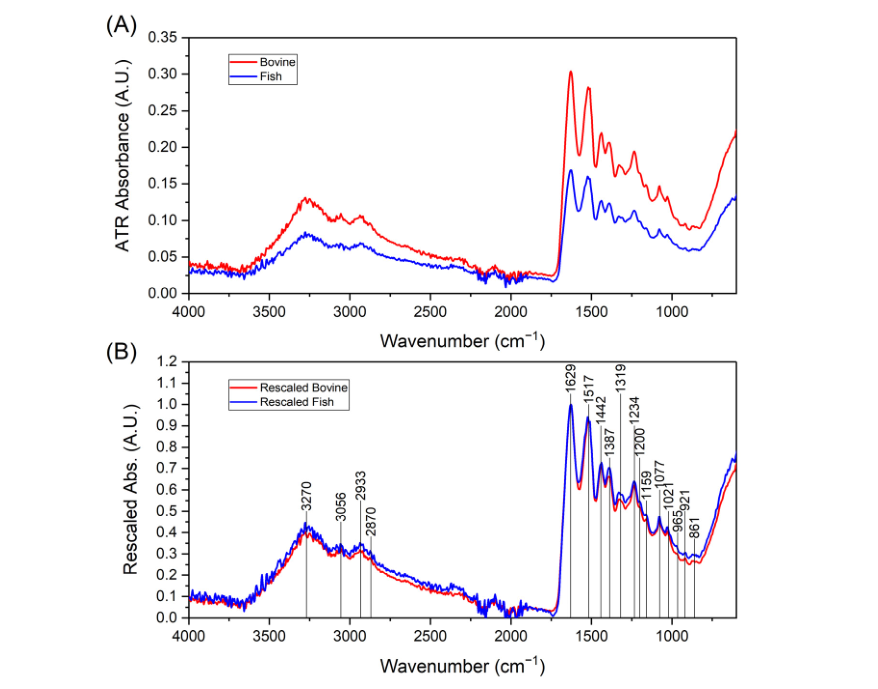
图1 (A)Coll₆和Collᵦ粉末样品的FTIR光谱;(B)经缩放后的FTIR光谱及相关吸收峰标识(注:缩放方法为扣除背景后,以1629 cm⁻¹共有的最强峰强度归一化)
两种胶原肽的FTIR光谱无显著化学结构差异,主要吸收峰位置一致:3250 cm⁻¹、1500–1600 cm⁻¹、500 cm⁻¹,符合胶原蛋白特征吸收区间(700–1700 cm⁻¹、2800–3500 cm⁻¹)。通过二阶导数分析定位的吸收峰,可归属为多肽特征化学键振动(见表1),仅部分峰的相对强度存在微小差异(归因于氨基酸组成差异)。
| 波数 [cm⁻¹] | 化学键振动模式(拉伸ν/面内弯曲δ) |
|---|---|
| 861 | ν(C-O)、ν(C-H)、δ(C-O-H)、δ(C-O-C) |
| 921 | ν(C-O)、ν(C-H)、δ(C-O-H)、δ(C-O-C) |
| 965 | ν(C-O)、ν(C-H)、δ(C-O-H)、δ(C-O-C) |
| 1021 | ν(C-O) |
| 1077 | ν(C-O) |
| 1200 | δ(N-H)、ν(C-N) |
| 1234 | δ(N-H)、ν(C-N) |
| 1319 | δ(CH₂)、δ(N-H)、ν(C-N) |
| 1387 | δ(CH₂)、δ(CH₃) |
| 1442 | δ(CH₂)、δ(CH₃) |
| 1517 | δ(N-H)、ν(C-N) |
| 1629 | ν(C=O) |
| 2870 | ν(C-H)、ν(CH₃) |
| 2933 | ν(C-H)、ν(CH₂)、ν(O-H) |
| 3056 | ν(C-H)、ν(N-H)、ν(O-H) |
| 3270 | ν(O-H) |
| 3322 | ν(N-H) |
表1 胶原肽FTIR吸收峰位置及对应化学键振动模式
(2)生物墨水流变学表征
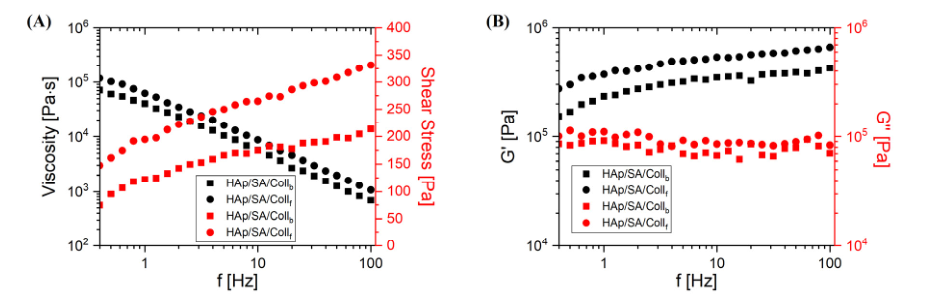
图2 溶液在0.4–100 Hz频率范围内的流变学表征:(A)黏度与剪切应力;(B)储能模量(G')与损耗模量(G'')
① 频率<0.3 Hz时,两种墨水测试数据不稳定(黏度随机骤降),故仅分析0.4–100 Hz数据;② 两者均为非牛顿剪切变稀流体:频率升高时,黏度显著降低,剪切应力明显升高;其中Coll₆基墨水黏度略高于Collᵦ基墨水;③ 黏弹性:两者均表现为"类固体行为"(全频率范围G'>G''),G'随频率适度升高,G''基本不随频率变化;该特性保障挤出时细丝结构完整性。
(3)可打印性评估
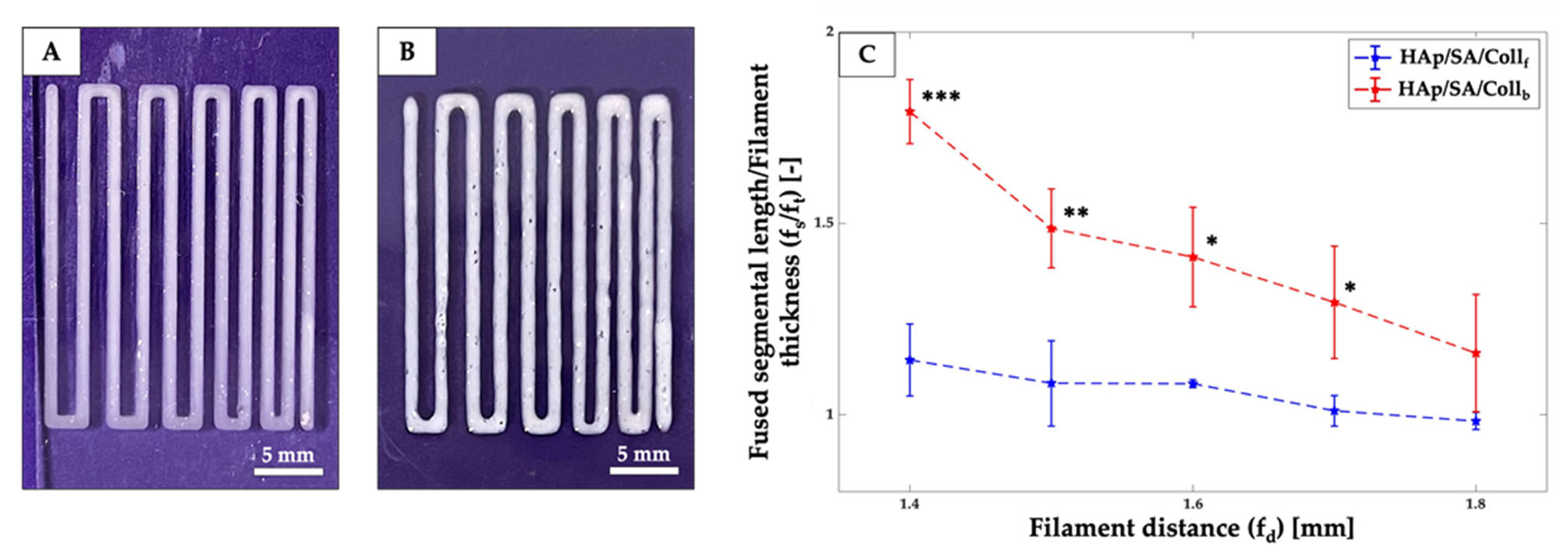
图3 (A)HAp/SA/Coll₆墨水、(B)HAp/SA/Collᵦ墨水的细丝融合测试结果;(C)两种墨水的fₛ/fₜ与f_d关系图(***p≤0.001,**p≤0.01,*p≤0.05)
细丝融合测试:相邻细丝存在轻微融合趋势,且随间距(f_d)减小更显著;f_d=1.4 mm(最小间距)时,HAp/SA/Coll₆墨水的fₛ显著低于HAp/SA/Collᵦ墨水(p≤0.001),表明其打印分辨率更优,可构建更精细结构。
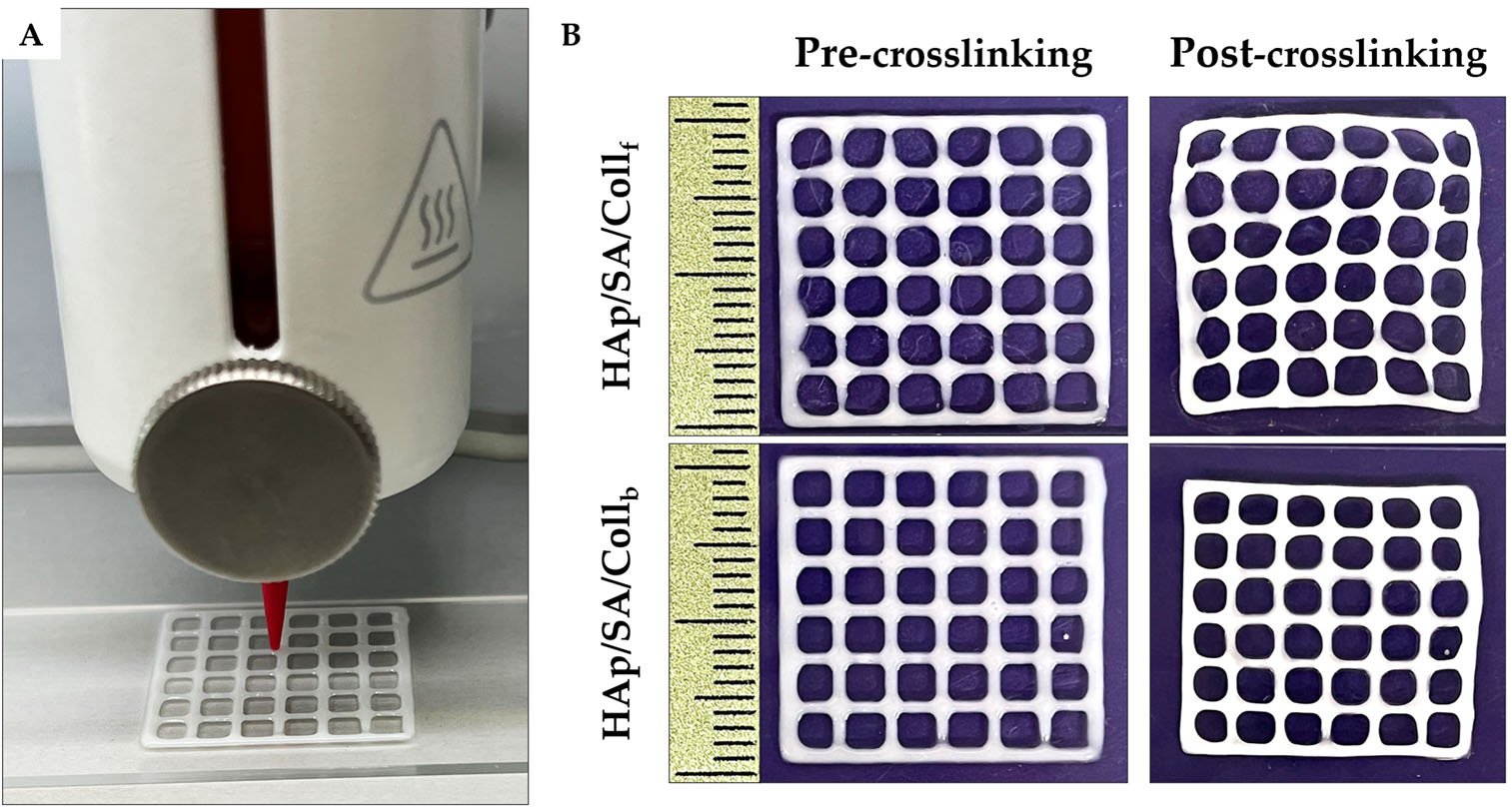
图4 (A)HAp/SA/Coll基墨水打印20×20×0.6 mm³方格的过程;(B)两种墨水打印方格在交联前后的可打印性评估
| 墨水类型 | 可打印性(Pᵣ) | 扩散率(Dᵣ) | 收缩率(S, %) |
|---|---|---|---|
| HAp/SA/Coll₆ | 0.82±0.01 | 39.51±3.41 | 13.62±1.41 |
| HAp/SA/Collᵦ | 0.85±0.01 | 43.72±3.39 | 12.88±0.85 |
表2 两种生物墨水的可打印性评估参数(均值±标准差;Pᵣ:可打印性,Dᵣ:扩散率,S:收缩率)
方格结构打印:① 两种墨水Pᵣ均接近1.0(良好可打印性),HAp/SA/Collᵦ墨水的Pᵣ(0.85±0.01)显著高于HAp/SA/Coll₆墨水(0.82±0.01,p≤0.001),表明其孔隙可打印性更优;Pᵣ<1.0均因墨水轻微欠凝胶化,导致孔隙呈圆形而非方形;② 扩散率(Dᵣ):HAp/SA/Coll₆墨水的Dᵣ(39.51±3.41)显著低于HAp/SA/Collᵦ墨水(43.72±3.39,p≤0.01),说明其细丝扩散更少,孔隙闭合效应更弱,几何保形性更优;③ 收缩率(S):两种墨水收缩率均较低,HAp/SA/Collᵦ墨水的S(12.88±0.85%)略低于HAp/SA/Coll₆墨水(13.62±1.41%),交联后形状保留更优。