近日,中国药科大学药学院周建平教授、丁杨教授团队在国际顶级期刊《Advanced Functional Materials》(IF=19)发表题为“Kinetics-By-Design:On-Demand Fabrication of Personalized Drug-Release Profiles Using Multi-Material 3D Printing”的研究论文。该论文第一作者为陈培鸿,与深圳森工科技有限公司联合创办了深圳元一智慧医药科技有限公司,专注于3D打印药物智能设计与制造领域,持续推动3D打印技术在医药领域的研究和应用。森工科技(元一智慧)为本次研究的顺利推进提供了重要的技术与资源支撑。森工科技(元一智慧)AutoBio2000直接墨水书写(DIW)药物3D打印机作为核心实验设备,全程助力团队构建“动力学设计”三维框架,实现高水溶性窄治疗指数(NTI)药物的个性化、可编程释放,为精准药学研究提供了革命性技术方案。
研究背景:破解高水溶性NTI药物释放难题
在当今的医疗领域,精准给药一直是科学家们追求的目标。尤其是对于治疗指数窄(NTI)的药物,如4-氨基吡啶(4-AP),微小的血浆浓度变化都可能导致治疗失败或毒性反应。传统的给药方式往往难以满足个性化治疗的需求,而3D打印技术的出现为这一难题带来了新的解决方案。目前,4
-
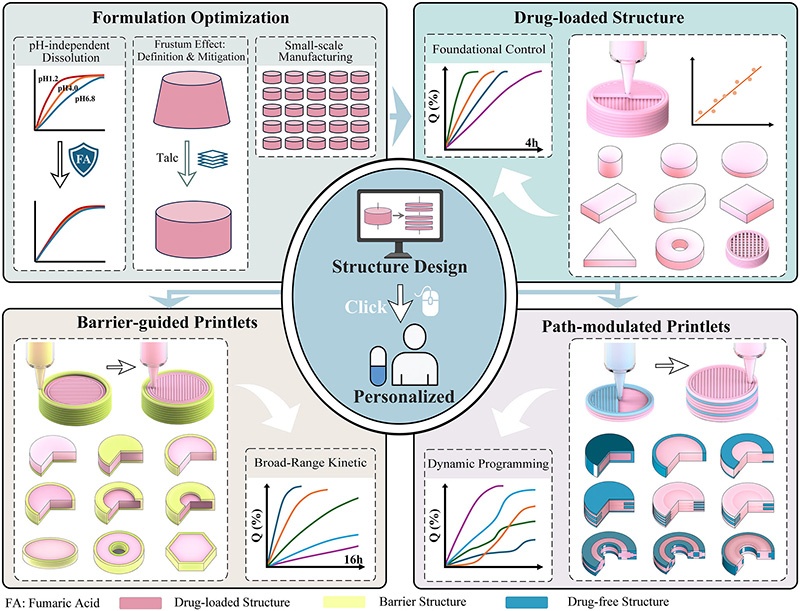
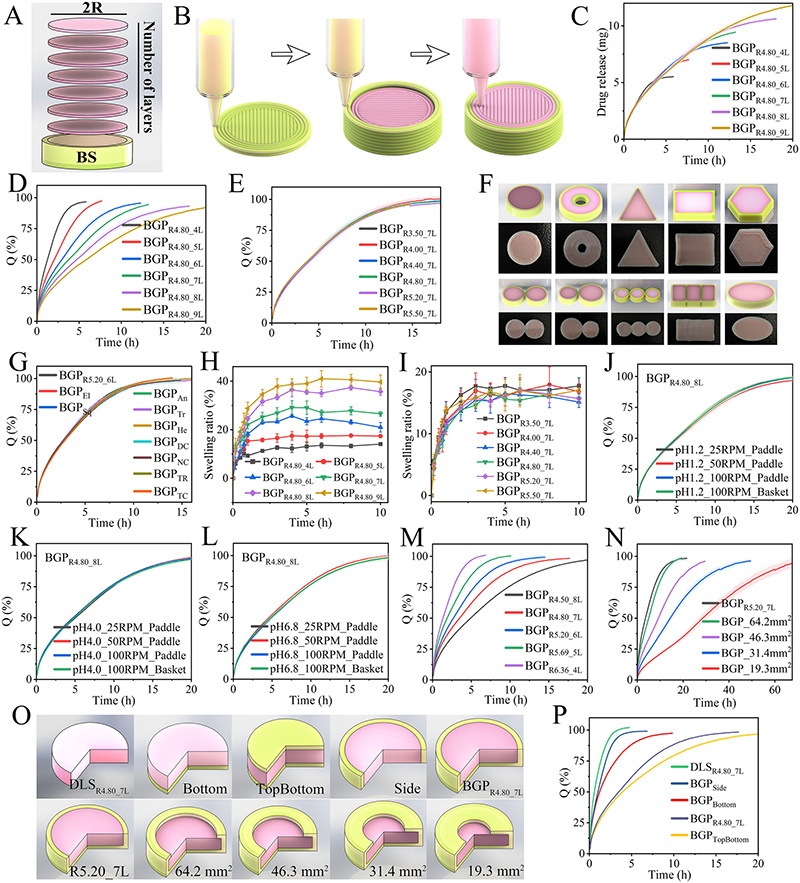
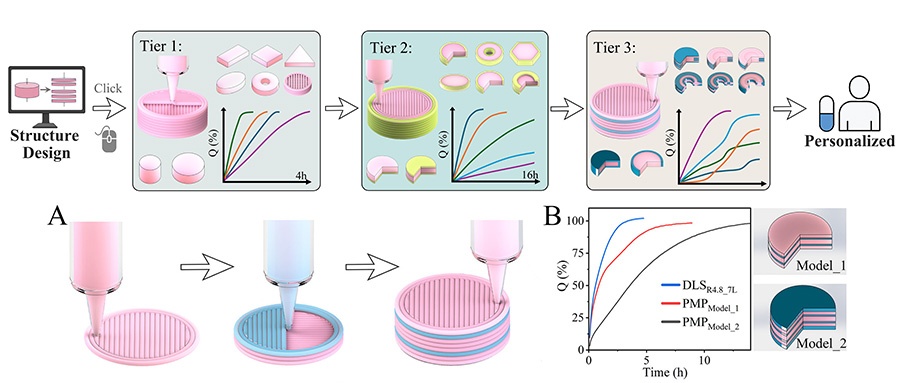
AP的给药方式存在明显的局限性。速释制剂往往会导致血浆浓度出现急剧峰值,增加了癫痫发作的风险;而缓释制剂虽然降低了这种风险,但只能提供固定的、千篇一律的释放曲线。这种设计无法适应患者之间的个体差异,也无法为慢性肾病等脆弱人群提供更复杂、适应性更强的释放曲线。因此,目前缺乏一种可扩展的平台,能够超越剂量个性化,实现按需定制动态编程的释放动力学。另一方面,高水溶性药物的给药也面临着挑战。虽然高水溶性有助于药物的吸收,但也使得药物释放动力学难以精确控制。在传统的剂型中,水溶性药物均匀分散在基质中,释放行为主要由药物的内在理化性质(如溶解度、pH敏感性和离子化程度)决定,难以对溶解的中间阶段进行调节,实现精确、可编程的释放曲线仍然是一个重大挑战。传统的制药工艺主要依赖于迭代的制剂和工艺优化来控制水溶性药物的释放曲线,这种方法不仅劳动强度大、耗时久,而且不适合快速个性化给药。3D打印技术的出现为解决这一问题带来了新的希望。它有望将释放控制从制剂转移到结构上。然而,目前的3D打印策略仍存在一些局限性。首先,即使在复杂的打印几何形状中,药物通常均匀分布在基质中,释放行为仍然受API的内在溶解速率支配,无法在中间阶段进行微调。也就是说,大多数当前的3D打印系统在组成上本质上仍然是均匀的,因此,3D打印利用空间分辨的多材料架构实现复杂释放控制的潜力尚未得到充分发挥。其次,一些先进的设计,如带通道的制剂,试图通过调节流体动力学来影响释放,但这种策略可能是一把双刃剑。许多这样的系统采用可侵蚀基质,在溶解过程中会发生溶胀或结构损失,这些变化会动态改变表面积与体积(SA/V)比,破坏局部流体动力学,使释放曲线难以预测。即使在非侵蚀性基质中,外部通道也容易被食物颗粒或胃肠道内容物堵塞,导致进一步的变异性。基于此,团队创新性地提出“以结构编码释放动力学”的核心思路,借助森工科技(元一智慧)AutoBio2000的多材料打印能力,将药物释放的控制权从传统的“制剂组成”转移到“空间结构”上,突破了配方依赖的传统研发模式。图1:“动力学设计”三层框架示意图。左上展示在DLS内部构建稳定微环境,对干燥引发的截头体变形通过角度θ进行质量分级并优化,实现小批量稳定制造;右上为通过对表面积/体积比的调节,可实现释放个性化并构建预测模型;左下为BGPs,通过构建惰性屏障层实现各向异性扩散,并实现16h内的释放个性化调节;右下为PMPs,内部嵌入药物自由结构(DFS)作为“动力学门”,可实现滞后时间调整与加速-减速阶段动态控制,产生分段多阶段释放曲线,满足个性化给药需求。
“动力学设计”三层框架总述
“动力学设计”是一种创新的药物释放控制策略,它以多材料3D打印技术为支撑,构建了一个三层框架,旨在通过结构而非组成来精确控制药物释放,为个性化药物治疗提供了全新的解决方案。该框架以4
-
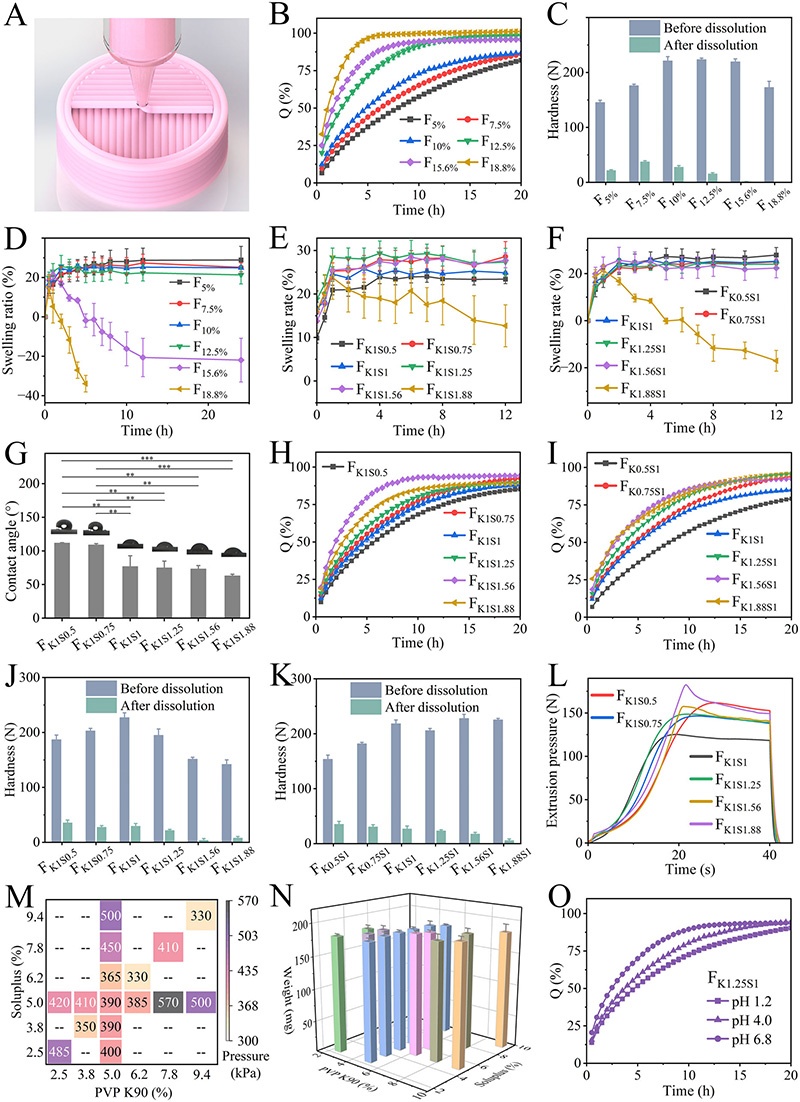
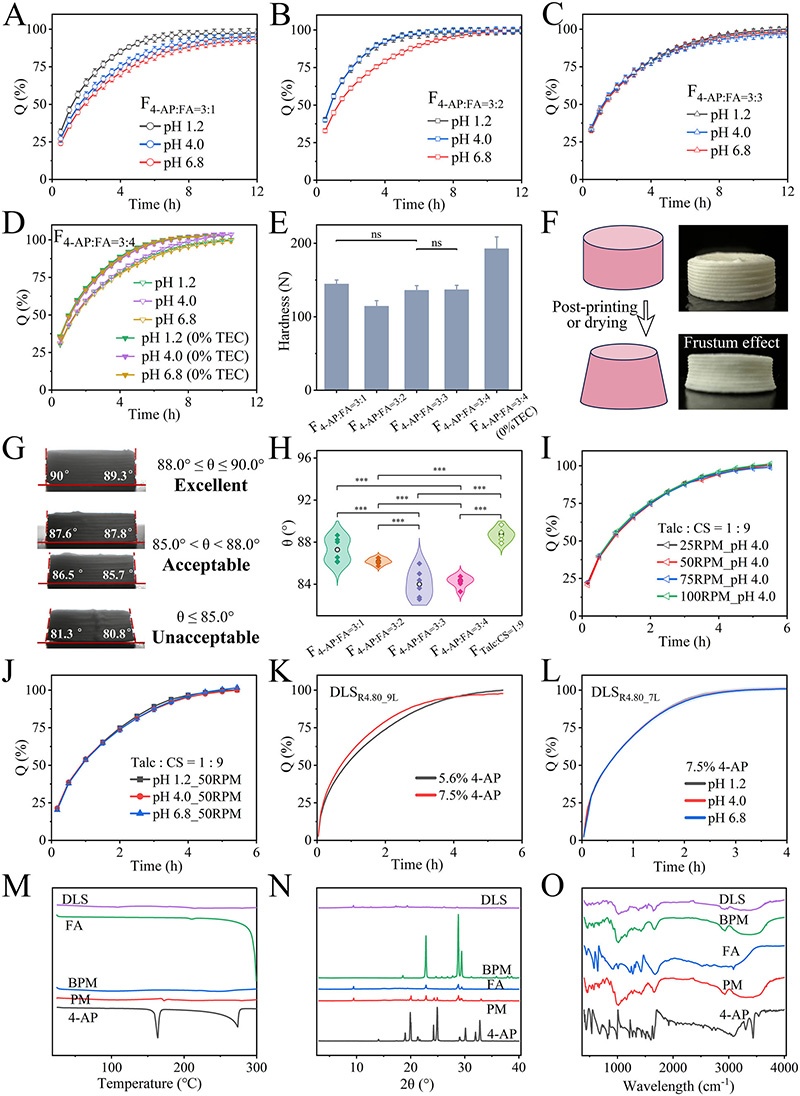
AP为模型药物,针对高水溶性和pH敏感性药物的释放难题,进行了系统性的研究和设计。第一层的载药结构(DLS)作为基础单元,通过合理的配方设计和工艺优化,消除了pH依赖性,解决了干燥引起的圆台体效应,实现了高度可重复的制造。该结构具有良好的机械强度和药物释放特性,可通过调节表面积/体积比在4小时内实现个性化释放。第二层的屏障引导型制剂(BGPs)引入了各向异性扩散,将路径长度和释放面积转化为可编程变量。通过多材料3D打印技术,在药物负载结构外部构建惰性屏障层,形成单向释放路径,实现了8 - 20小时的可预测持续释放,且释放曲线符合通用模型(R² = 0.992)。第三层的路径调制型制剂(PMPs)则进一步引入了内部“动力学门”,通过在药物负载结构内部嵌入药物自由结构,实现了滞后时间调整和加速-减速阶段的动态控制。这种设计使得药物释放曲线更加灵活多样,能够满足复杂的临床治疗需求,为个体化治疗提供了更精准的手段。总体而言,“动力学设计”三层框架通过巧妙的结构设计和先进的3D打印技术,将药物释放从传统的制剂依赖转变为结构可控,为解决高水溶性和pH敏感性药物的释放难题提供了有效的途径,有望推动个性化药物治疗的发展,为患者带来更好的治疗效果和生活质量。图2:DLS的配方筛选与优化结果。包括不同Soluplus和PVP K90含量对DLS溶解性能、机械强度、溶胀性能、表面润湿性、墨水挤出压力、打印压力和药片重量一致性的影响,以及不同pH条件下的溶解曲线。图3:DLS的环境稳定性和制造保真度。展示了不同FA含量对DLS在不同pH介质中溶解曲线的影响,TEC去除对DLS溶解性能和机械强度的影响,截头体效应的量化评估和解决方法,不同桨速和pH条件下DLS的溶解曲线,药物负载量对DLS释放速率的影响,以及DSC、PXRD和FT
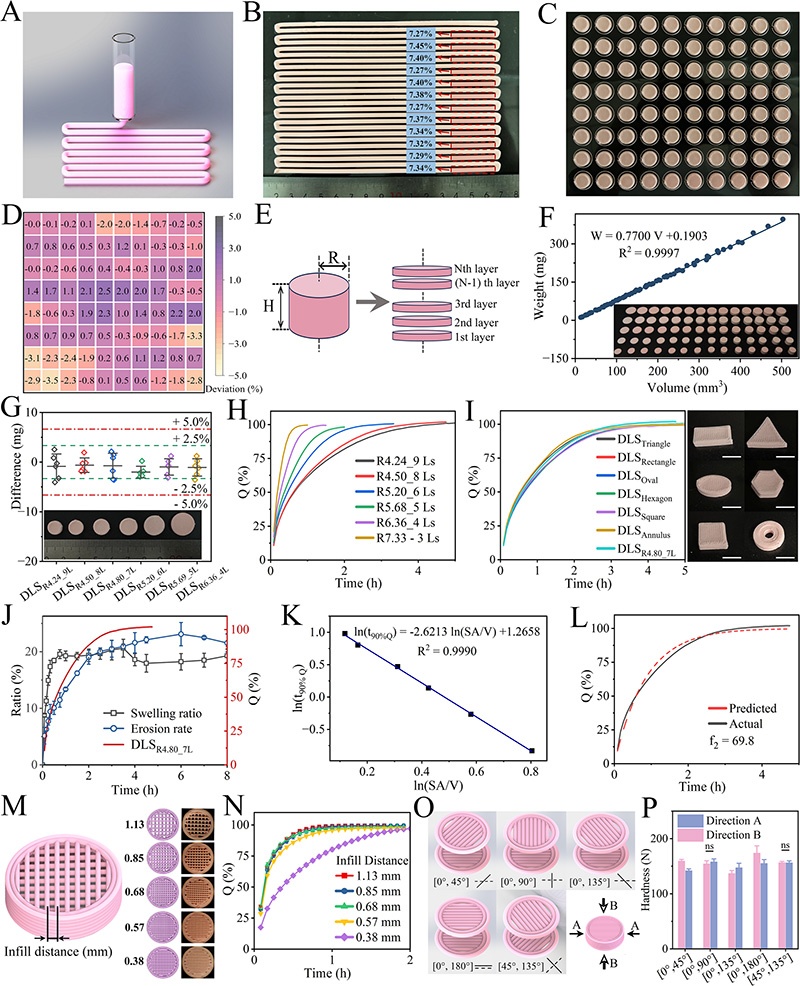
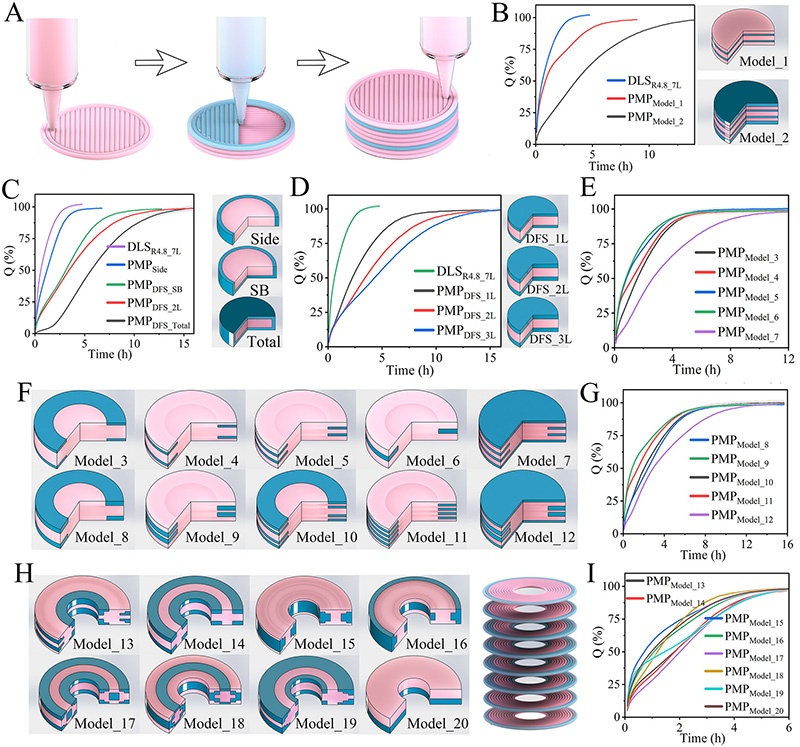
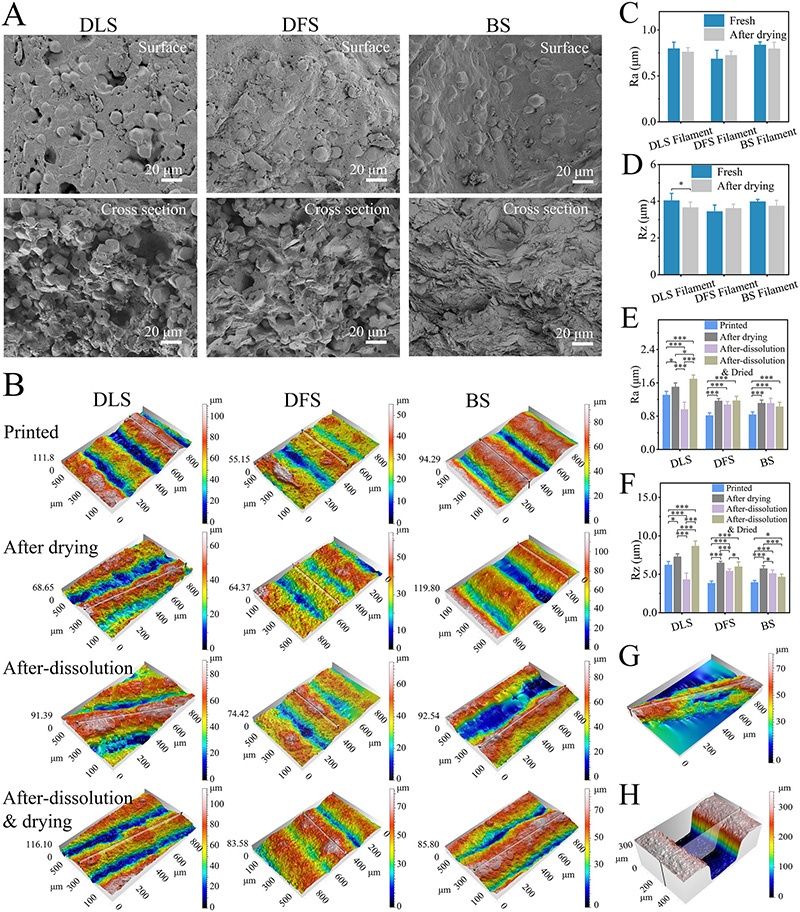
- IR分析结果。图4:DLS质量控制与动力学建模。体积-重量线性回归R²=0.9997,SA/V比是释放动力学的主导因素;填充角度[0°,90°]和[45°,135°]配置确保机械强度的各向同性。图5:BGPs实现长期个性化释放。展示了BGPs的单向释放原理和制备过程,不同释放面积和扩散路径的BGPs的溶解曲线和溶胀曲线,不同几何形状但相似表面积的BGPs的溶解曲线,不同pH和桨速条件下BGPs的溶解曲线,以及通过改变BGP结构实现的按需个性化溶解曲线。图6:PMPs的动态释放特性。展示了不同“动力学门”设计下PMPs的动态释放曲线,包括滞后时间、加速-减速阶段等。通过对比不同设计的PMPs的释放曲线,直观地呈现了PMPs实现全轮廓控制的能力,以及“动力学门”对药物释放的精确调控作用。图7:制剂的微观结构及其在加工和溶解过程中的动态演变。展示了DLS、DFS和BS的表面和横截面的SEM图像,揭示了它们不同的微观结构;不同阶段(打印后、干燥后、释放后、释放后再干燥)的DLS、DFS和BS的3D表面形貌;DLS、DFS和BS在干燥前后的算术平均粗糙度(Ra)和最大轮廓高度(Rz)变化;打印后、干燥后、溶解后及溶解后再干燥的DLS、DFS和BS的表面粗糙度参数;以及打印过程中可能出现的缺陷(如气泡引起的表面塌陷或丝断裂)的3D表面形貌。通过多尺度成像方法,阐明了宏观水平的制剂性能与其微观结构之间的联系。
应用价值与未来展望
“动力学设计”框架为个性化医疗和药物研发带来了突破。在个性化医疗领域,它能够根据患者的个体差异定制药物释放曲线,实现精准给药,有效解决了治疗指数窄药物的毒性反应和治疗失败风险。同时,通过实现药物的持续释放,提高了患者的依从性,有助于更好地控制慢性疾病。在药物研发领域,该框架可以加速新药研发进程,通过计算机模拟和3D打印技术快速制备和测试药物制剂,缩短研发周期。此外,它还解决了高水溶性和pH敏感性药物的释放难题,拓展了这些药物的适用范围,降低了医疗成本,提高了医疗效率。未来团队将整合AI驱动建模与过程分析技术,进一步实现临床级个性化药物的规模化生产。
论文链接:https://doi.org/10.1002/adfm.202527954
第一作者:陈培鸿(15992585225@163.com)
通讯作者:周建平、丁杨